B細胞慢性リンパ球性白血病
慢性リンパ球性白血病は、成熟リンパ球ががん化し、徐々にリンパ節の正常な細胞に取って代わる疾病で、患者の4分の3以上が60歳を超えており、小児にはみられない。また、男性では女性の2~3倍多い。北米とヨーロッパでは最も多い種類の白血病であるが、日本と東南アジアではまれである。
疾病の経過とともに、肝臓と脾臓に広がり、これらの臓器が腫れる。悪性リンパ球は骨髄にも侵入、正常細胞と置き換わる。その結果、血液中の赤血球が減少し、正常な白血球と血小板の数も減少する。慢性リンパ球性白血病の95%がB細胞のがんである。
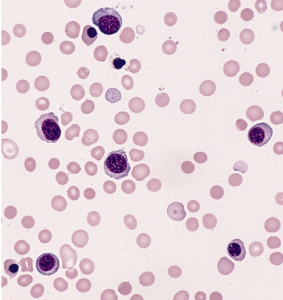
(画像はウィキメディア)
第3相試験の中止
セルジーン・コーポレーションは米食品医薬品局(FDA)と協議した結果、第3相非盲検試験ORIGIN8におけるレブラミド(レナリドミド)による治療を中止すると発表した。
本試験はB細胞慢性リンパ球性白血病を有する年齢65歳以上の高齢患者で、フルダラビンやベンダムスチンを含むレジメンなど、より積極的な標準的化学免疫療法による治療が不可能となる併存疾患を有する患者に対し、単独療法としてのレナリドミドの有効性と安全性をクロラムブシルと比較して評価する試験であった。26カ国100以上の施設で450例の患者を組み入れた。クロラムブシル治療群において患者211例中18例が死亡したのに対して、レナリドミド治療群において患者210例中34例が死亡したことに基づき、死亡数に不均衡がみられたとしてFDAはORIGIN試験の実施保留命令を出した。(堤朝子)
▼外部リンク
QLifePro Press 2013年7月22日
https://www.qlifepro.com/press/




