シナプスの変化に小脳から分泌される「Cbln1」が関与
慶應義塾大学は5月7日、シナプスを新しく作り出す働きを持つタンパク質「Cbln1」が、神経活動に応じてタンパク質を分解する酵素をもつ細胞内小器官・ライソソームから分泌されることを、マウスを用いた実験により明らかにしたと発表した。この研究は、同大医学部生理学教室の柚﨑通介教授、聖マリアンナ医科大学生理学教室の井端啓二助教、幸田和久教授らによるもの。研究成果は、米国科学雑誌「Neuron」にオンライン速報版で公開された。
画像はリリースより
神経回路網を形成するシナプスは、遺伝情報に基づいて形成されるのみではなく、生後の環境因子や、経験・学習によって生涯にわたり機能的にも形態的にも変化を受け続ける。そのため、神経活動に応じたシナプス再編過程を理解することは、シナプスに病変が存在するうつ病・統合失調症などの精神疾患や、自閉スペクトラム症などの神経発達症、さらに、アルツハイマー病をはじめとする認知症などの神経疾患の病態解明と、新たな治療方法開発のために、極めて重要な課題とされている。
研究グループはこれまでに、免疫系で異物を認識する補体に似た補体ファミリー分子のCbln1が小脳の顆粒細胞から分泌され、シナプス形成過程を制御することを報告していた。さらに、Cbln1欠損マウスでは、シナプスの数が激減し、運動失調や運動学習の障害が生じることをこれまでの研究報告で明らかになっていたが、どのようにして神経活動がシナプスの変化につながるのか、その過程にCbln1が関与しているのかなど、その分子機構については、不明な点が多く残っていた。
Cbln1が顆粒細胞の表面のみでなく、ライソソームに存在すると判明
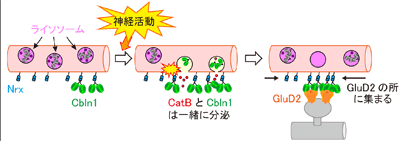
研究グループは今回、Cbln1が顆粒細胞の内部のどこに存在するかを調査。その結果、Cbln1は顆粒細胞の表面のみでなく、不要なタンパク質や老廃物を分解するための細胞内小器官である「ライソソーム」に存在することが判明した。また、神経活動が亢進すると、軸索からライソソームの内容物(タンパク質分解酵素とCbln1)が細胞外に分泌されることも初めて明らかにされた。
細胞外に放出されたCbln1は、平行線維上に存在するNrxに即座に結合したのち、平行線維に沿って拡散し、近接する細胞上に存在するGluD2と出会うと、その場所に集積した。Cbln1はこのようにして、GluD2を発現するプルキンエ細胞の樹状突起に集積し、シナプス形成を引き起こすと考えられるという。また、ライソソームから細胞外への分泌過程を阻害したところ、神経活動依存的なCbln1とCatBの細胞外への分泌が抑えられるとともに、マウス小脳においてシナプスのもととなる部分の数が減少することも判明した。
精神疾患や神経発達症の病態理解、新たな治療法創出に期待
今回の研究成果により、タンパク質分解酵素による細胞外環境の破壊(スクラップ)と、Cbln1によるシナプス形成(ビルド)が、協調して働くことによって、神経活動に応じたシナプスの再編が起きる可能性が示唆されたこととなる。
シナプス再編は記憶・学習の実体であり、その障害は多くの精神疾患や神経発達症で報告されている。研究グループは、「本研究をさらに発展させることによって、これらの疾患の病態や新しい治療法の創出につながることが期待される。また、アルツハイマー病などの神経変性疾患においては、変性タンパク質がライソソームから分泌されて、周りの神経細胞に伝播していく可能性も示唆されている。したがってライソソーム分泌機構の解明は、ライソソームをターゲットとした治療法の創出にもつながることが期待できる」と、述べている。
▼関連リンク
・慶應義塾大学 プレスリリース



