アルギニンメチル化を指標としたヒストン変化を解析
東京医科歯科大学は12月4日、胃がんにおいて、ヒストン修飾に関わるPRMT6が活性化し、がん抑制遺伝子のPCDH7が不活化していることを世界で初めて明らかにしたと発表した。この研究は、同大大学院医歯学総合研究科分子腫瘍医学分野の田中真二教授、秋山好光講師、島田周助教、奥野圭祐大学院生らの研究グループが、同ウイルス制御学の山岡昇司教授、同低侵襲医療学の小嶋一幸前教授(現・獨協医科大学第一外科主任教授)と共同で行ったもの。研究成果は、国際科学誌「Carcinogenesis」オンライン版で発表されている。
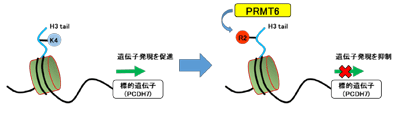
画像はリリースより
ヒストン修飾はエピジェネティックな遺伝子発現機構のひとつで、多くの疾患の発生に重要な役割を果たしている。ヒストンH3のリジン残基(K)はメチル化やアセチル化などの翻訳後修飾を受けることで遺伝子発現活性化・不活性化の調節に関与しているが、悪性腫瘍ではヒストン修飾状態が変化しており、また、リジンメチル化を触媒するヒストンメチル化酵素やヒストン脱メチル化酵素の異常も相次いで報告されていることから、ヒストン修飾を指標とした治療薬の開発が国内外で展開されている。
胃がんにおけるDNAメチル化やヒストンリジンメチル化・アセチル化の解析も多くの施設で行われてきたが、アルギニンメチル化を指標としたヒストン変化の解析は行われていなかった。
PRMT6-H3R2me2as経路により、がん抑制遺伝子PCDH7が不活化
研究グループは、ヒト胃がんの臨床症例を用いた解析で、ヒストンH3のアルギニンの非対称性メチル化(H3R2me2as)レベルとその主要酵素であるPRMT6の発現が、ともに胃がんで亢進していることを解明。また、臨床的には、高H3R2me2asレベルは胃がんの独立した予後因子であり、かつ両方の発現が強い胃がんは再発しやすく死亡する割合が高いことを見出した。次に、ヒト胃がん細胞を用いてPRMT6安定発現細胞株を作成したところ、H3R2me2asのレベルが亢進し、腫瘍細胞の遊走能や浸潤能が亢進。一方、ゲノム編集法を用いてヒト胃がん細胞でPRMT6をノックアウトすると、H3R2me2asのレベルが減弱し、腫瘍の増殖能、遊走能、浸潤能および造腫瘍能も低下したという。
遺伝子の活性化にはヒストンH3の4番目リジン(K4)のトリメチル化(H3K4me3)が強く相関している。胃がん細胞でPRMT6発現が強くなると、H3R2は特異的に非対称性メチル化され、H3K4me3レベルが減少することで、遺伝子発現が抑制されることが明らかになった。このメカニズムを通してPRMT6によってがん抑制遺伝子PCDH7など複数の遺伝子発現が負に制御されていた。PRMT6をノックアウトした胃がん細胞ではPCDH7発現は亢進したが、その発現を再び抑えると、腫瘍細胞の遊走能と浸潤能が回復することが判明。したがって、胃がんではPRMT6-H3R2me2as経路によってPCDH7の発現が抑制され、悪性度が増強していることが示唆された。
今回の結果から、胃がんにおいてH3R2me2asはPRMT6発現と正に相関すること、および予後予測のバイオマーカーになる可能性が示唆された。また、PRMT6-H3R2me2as経路によって、がん抑制遺伝子のPCDH7が不活化していることを世界で初めて明らかにした。研究グループは、「胃がんで発現亢進しているPRMT6を抑えると、悪性度や造腫瘍性が抑えられた成果は、PRMT6異常を標的とした新規治療法開発につながることが期待される」と述べている。
▼関連リンク
・東京医科歯科大学 プレス通知資料



