小脳萎縮による運動障害などが見られる希少疾患、有効な治療法は未開発
島根大学は8月7日、重度の小脳失調および認知機能障害などを呈する乳児期発症神経変性症(childhood-onset neurodegeneration with cerebellar atrophy:CONDCA)の治療法の開発のために、マウスを用いた遺伝子治療研究を行ったと発表した。今回の研究は、同大医学部生理学講座の桑子賢一郎准教授、医学部附属病院病理部の荒木亜寿香准教授らの研究グループによるもの。研究成果は、「Molecular Therapy」にオンライン掲載されている。
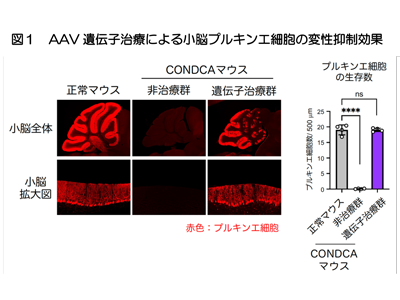
画像はリリースより
(詳細は▼関連リンクからご確認ください)
CONDCAは米・独・仏の合同研究グループによって2018年に初めて報告された重篤な遺伝性小児神経変性疾患である。同疾患は主に乳児期に発症し、病名の通り、小脳萎縮による運動障害を特徴とし、さらに、認知機能障害や発達遅延などを呈する。また、CONDCA患者は発育期に死亡することも少なくない。CONDCAは、細胞骨格の修飾酵素Cytosolic carboxypeptidase 1(CCP1)をコードするAGTPBP1遺伝子の変異に起因することが知られているが、これまでCONDCAの治療法開発のための研究はほとんどなく、実際、有効な治療法はまだ存在していない。
CONDCAモデルマウス作製と小型化CCP1タンパク質による遺伝子治療開発
CONDCAは、疾患遺伝子変異によってCCP1タンパク質の機能が消失あるいは低下することで発症すると考えられている。そこで、研究グループは、まず、生体内ゲノム編集技術によってAGTPBP1遺伝子を欠失させたCONDCA疾患モデルマウスを作製した。そして、このマウスは、CONDCA患者と同様に、小脳機能に必須の神経細胞(プルキンエ細胞)が生後発育期に変性して脱落し、また、顕著な運動障害を呈することがわかった。
次に、これらの小脳病変を指標にAAVベクターによる遺伝子治療の効果を検証した。当初、研究グループはAAVベクターによって全長型のCCP1をCONDCAマウスの神経細胞に発現させて失われた機能を補填する戦略を検討した。しかし、AAVベクターに搭載できる外来遺伝子サイズには制限があり、AGTPBP1遺伝子はその制限を大きく超えていた。そこで、まず、酵素活性に不要な部分を削った”小型”のCCP1タンパク質を同定し、さらに、その小さなCCP1を簡便な静脈注射によって脳内全域の神経細胞に発現させることができるAAVベクターを構築した。
開発した遺伝子治療、疾患マウスのプルキンエ細胞脱落を抑制・小脳失調症状を改善
そして、発症前のCONDCA新生仔マウスに、上述のCCP1を発現するAAVベクターを経静脈投与し、プルキンエ細胞の生存と運動機能を調べた。その結果、CONDCAマウスで見られるプルキンエ細胞の著しい脱落が大きく抑制されていることが明らかになった。さらに、CONDCAマウスが呈する小脳失調症状である歩行中の転倒やよろめきの回数が、遺伝子治療によって劇的に減少することもわかった。
以上のことから、AAVベクターを用いた遺伝子治療がCONDCAの治療法として有用である可能性が初めて示された。
CONDCA遺伝子治療の有用性を示唆、課題克服により治療実現につながると期待
今回の研究により、CONDCAに対する遺伝子治療の有用性が初めて示された。この成果は、同疾患の今後の治療戦略の基盤として非常に重要な知見になると考えられる。一方、今回の遺伝子治療ではCONDCAマウスの自発運動中の安定性が向上したが、すべての運動機能が改善したわけではない。また、CONDCAのもう1つの主症状である認知機能障害については評価がなされていない。従って、今後はAAVベクターの改良や投与方法の検討とともに、他の症状についても治療効果を調べていくことが重要になる。「これらの課題を克服できれば、CONDCAの治療が実現し、患者の病態を大きく緩和できると期待される」と、研究グループは述べている。
▼関連リンク
・島根大学 プレスリリース



