ALS原因タンパク質の異常凝集、液-液相分離現象の関与が指摘されている
東北大学は11月5日、筋萎縮性側索硬化症(ALS)の原因タンパク質が細胞内で固まる(凝集する)のを、RNAがどのように防ぐかを明らかにしたと発表した。この研究は、同大大学院薬学研究科の小倉泰成大学院生、松浦宇宙大学院生(研究当時)、田原進也助教、中林孝和教授らの研究グループによるもの。研究成果は、「JACS Au」に掲載されている。
画像はリリースより
(詳細は▼関連リンクからご確認ください)
ALSは神経変性疾患の一つであり、運動神経細胞が機能を失うことで呼吸や手足の運動が困難になる疾患である。ALSの根本的な治療法や予防法はまだ確立していない。ALSは神経細胞内におけるFused in sarcoma(FUS)やTDP-43などといったタンパク質が異常に固まり(凝集する)、神経細胞に障害を引き起こすことで生じると考えられている。こうしたタンパク質の異常な凝集を防ぐことができれば、ALSの治療や予防につながると期待される。
これらのALS原因タンパク質の凝集が、「液-液相分離(LLPS)」という現象によって促進されることが近年指摘されている。LLPSは、タンパク質が高濃度に存在する液体状態(液滴)が溶液内で形成される現象である。通常、タンパク質は細胞内で分散した状態で存在しているが、細胞がストレスを受けると病原性タンパク質を含む生体分子が集合し、液滴を作る。この液滴から病原性タンパク質が固まってしまうことが示されている。
RNAが液滴の安定性を調整、そのメカニズムは未解明
さらに、細胞の中に豊富に存在するRNAが、この液滴の形成や安定性を調整していることが報告されている。しかし、RNAがどのようにLLPSを制御しているのかは未解明であった。RNAによるLLPSの制御機構を明らかにできれば、ALSの治療へと応用することができる。
RNAの「長さ」によって液滴の運命が変わることが判明
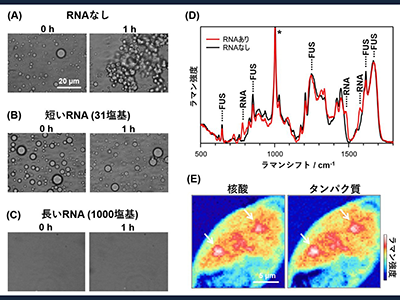
今回の研究では初めに、試験管内においてFUSの液滴を人工的に作成し、RNAをその液滴を含んだ溶液に加え、液滴の状態や凝集の進行を観察した。測定には、分子の状態をその場で観測できるラマン顕微鏡も用い、液滴の中にあるRNAやFUSの濃度や構造を解析した。
さまざまな特徴(配列・構造・長さ)のRNAを加え、液滴の形状変化を観察した。RNAを加えない場合、FUS液滴は約1時間で固まり始めた。50塩基以下の短いRNAを加えると、RNAの配列や構造に関係なく液滴は安定して保たれ、凝集が抑えられた。一方、1,000塩基を超える長いRNAを加えると液滴自体が消失した。以上より、RNAの「長さ」によって液滴の運命が変わることがわかった。
さらに、ラマン顕微鏡を用いて液滴内部の分子の状態を解析した。FUSの液滴に対して短いRNAを加えると、FUSの液滴内部にFUSだけではなくRNAの強い信号が観測された。この結果から、FUSの液滴内にRNAが自発的に濃縮されることで凝集を抑制することが示された。一方で長いRNAは液滴内部に取り込まれなかった。
液滴はタンパク質のみではなく、RNAを多量に含む
続いて、このようなRNAが本当に生細胞内のFUS液滴にあるのか検討した。FUS液滴は細胞にストレスを加えると生成することが知られている。細胞に浸透圧ストレスを与えたところ、細胞核および細胞質においてFUS液滴が生成した。
これらの液滴を、ラマン顕微鏡を用いて検討したところ、液滴がタンパク質のみではなく、RNAを多量に含むことを初めて明らかにした。
RNAがFUS液滴の凝集を抑制する役割を担っている可能性
さらに、同研究グループが以前に確立したラマン顕微鏡を使った生体分子濃度のその場定量法を用いて、液滴内の内在性RNAを定量したところ、液滴の内部の濃度が外側よりも2~3倍程度高いことがわかった。その濃度は試験管中に観測された液滴内のRNA濃度と概ね一致する。
同研究からRNAがFUSのLLPSを「長さ」に基づいて制御することを示した。短いRNAは液滴内のFUSに結合し、FUS同士の接触を妨害する「バッファー」の役割を果たすことで凝集を抑制し、長いRNAは液滴内に取り込まれなかったことから、液滴界面のFUSと結合することでFUSの親水性を高め、液滴内のFUS濃度を減少・消失させると考えられる。細胞内のFUS液滴もRNAを濃縮させていることから、RNAがFUS液滴の凝集を抑制する役割を担っていることが提案された。
RNAによるLLPS制御機構の解明が有効な薬剤設計につながる可能性
今回の研究により、RNAがFUS液滴のLLPSを制御する分子機構が明らかにされた。神経変性疾患にはALS以外にもアルツハイマー病やパーキンソン病などがあり、いずれの疾患においても特定タンパク質のLLPSが関わることが示されている。
「本研究グループでは、RNAがALS以外の疾患原因タンパク質のLLPSをも制御するのかを検証し、その分子機構を明らかにする研究を行っている。RNAによるLLPS制御機構を明らかにすることで、神経変性疾患に対する有効な薬剤設計の指針を提示できると考えている」と、研究グループは述べている。
▼関連リンク
・東北大学 プレスリリース・研究成果



