転写因子のRUNX1・RUNX2・RUNX3などの「RUNXファミリー」
京都大学は5月23日、造血に必須の多くの遺伝子を一括して制御する転写因子であるRunt-related transcription factor 1(以下、RUNX1)やRUNX2、RUNX3、補助因子のCBFβといったRUNXファミリーを包括的に抑制することで、RUNX1のみを抑制するよりも強い抗白血病効果を誘導することを発見したと発表した。この研究は、同大大学院医学研究科人間健康科学系専攻の森田剣ポスドク研究員、上久保靖彦准教授を中心とするグループが、理学研究科の杉山弘教授、医学研究科の足立壮一教授らと共に行ったもの。同研究成果は、米科学誌「The Journal of Clinical Investigation」にオンライン掲載されている。
画像はリリースより
RUNX1は、白血病の中で最も多いCBF白血病で「がん抑制遺伝子」として認識されており、RUNX1が強く抑制されることが白血病の発症・増殖・維持に重要な要素だと考えられてきた。しかし、先行研究によりRUNX1は「がん促進因子」としても機能し、治療ターゲットとなることも示されている。実際に、RUNX1の抑制には抗白血病効果があるものの、完全に白血病を制御することはできていない。
一方、骨発生に関する遺伝子を一括して制御する転写因子RUNX2は、白血病を含むさまざまながん腫でがん促進因子として認識されてきた。また、RUNX3は肺がんや胃がんでがん抑制遺伝子と考えられてきた。RUNX1、RUNX2、RUNX3は同じ特定の塩基配列に結合するが、がんにおける相互関係は不明であった。
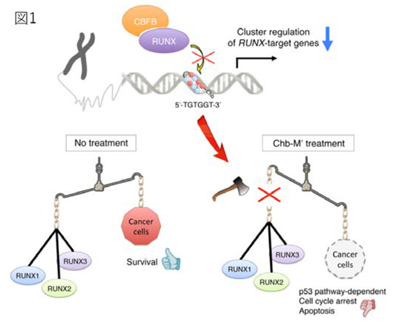
RUNXファミリーを包括的に抑制することで抗腫瘍効果を確認
そこで研究グループは、RUNX1、RUNX2、RUNX3の相互メカニズムと、包括的な抑制による抗腫瘍メカニズムの解明を目的として研究を実施した。まず、FLT3-ITD変異を持つMLL白血病細胞株でRUNX1の機能をノックダウンすると、がん抑制遺伝子p53が働き、がん細胞が死んでいくメカニズムを検証。その結果、RUNX1の働きを抑えると、p53を抑制していたTRIM24、BCL11Aがあまり働かなくなり、p53が機能し始めることがわかったという。また、この細胞抑制効果はp53の活性に左右されることも判明した。さらにRUNX1を単独でノックダウンした場合に比べ、RUNX2やRUNX3のノックダウンの追加やRUNX1、RUNX2、RUNX3の全てをノックダウンすることで、白血病細胞をさらに効果的に抑制することが明らかになったという。
次に、「Chb-M’」という、杉山教授が開発したalkylating agent-conjugated pyrrole-imidazole(PI)polyamides(PI-ポリアミド)を用いて、RUNXファミリーが制御する遺伝子群を包括的・人工的にスイッチオフし、更なる検証を行った。その結果、Chb-Mʼを使用した場合でも、極めて効率的に幅広いがん腫を抑制できることがわかったという。しかし、こちらでも抗腫瘍効果はp53 活性に左右されることが明らかになった。
最後に、各種ヒトがん細胞株を移植した免疫不全マウスにChb-Mʼを投与する実験を行った。現在、臨床現場で治療薬の第一候補として使用されている薬剤との治療効果比較を行ったところ、FLT3-ITD変異を持つMLL白血病治療モデルでは、Chb-Mʼを投与したグループの方が平均10日程度長く生存したという。また、チロシンキナーゼ阻害剤耐性PhALL白血病(フィラデルフィア染色体陽性急性リンパ性白血病)治療モデルでは、Imatinibの効果はほぼ確認できなかった。しかし、Chb-Mʼ投与群では約20日程度生存期間が延びたという。EGFR阻害剤耐性肺腺がん治療モデルやHer2胃がん治療モデルについても、Chb-Mʼは明らかな抗腫瘍効果を示した。さらに、正常マウスにChb-Mʼを投与した場合でも、ほとんど副作用が起こらず、24時間以内にほぼ血中より消失することを確認。Chb-Mʼは腫瘍にのみ集積する特徴を持つことも確認できたとしている。
研究グループでは毒性面などでの予備試験を行っており、今後さらにヒトに投与可能なグレードのChb-Mʼを用いた非臨床試験を進める予定だ。また、RUNXファミリーだけではなく、任意の類似機能を持つ塩基配列に結合するPI-ポリアミドのライブラリー開発も進行中。さまざまな塩基配列をターゲットとした新薬開発が可能であることから、今後PI-ポリアミドによる遺伝子スイッチテクノロジーは、新しい創薬の可能性を開くものとして期待される、と研究グループは述べている。
▼関連リンク
・京都大学 研究成果




