糖タンパク質を介した腫瘍微小環境の制御機構には未解明な点が多い
筑波大学は9月2日、乳がん転移を導く「がん細胞-免疫細胞間シグナル」を解明したと発表した。この研究は、同大医学医療系の川西邦夫助教(研究当時、現:昭和医科大学医学部解剖学講座顕微解剖学部門教授)、加藤光保教授らの研究グループによるもの。研究成果は、「PNAS(米国科学アカデミー紀要)」に掲載されている。
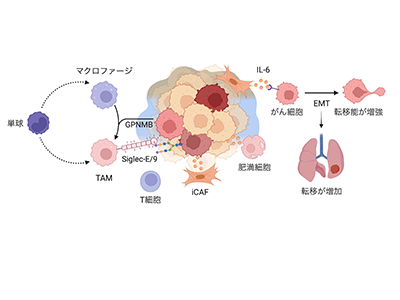
画像はリリースより
(詳細は▼関連リンクからご確認ください)
がんの進行や転移、治療抵抗性には、腫瘍微小環境(tumor microenvironment:TME)の動的な変化が深く関与している。TMEは、がん細胞のみならず、免疫細胞、間質細胞など多様な細胞種から構成され、それぞれが複雑に相互作用することで、がんの悪性化を促進する。中でも、腫瘍随伴マクロファージ(tumor-associated macrophages:TAM)は、TMEの中心的構成要素として、免疫抑制性の性質を持ち、がん免疫応答の回避に寄与することが知られている。
TAMは、がん組織に浸潤・定着し、炎症促進や免疫抑制など、がん種や進行段階に応じて幅広い機能的スペクトラムを持ち、免疫逃避、血管新生、転移促進に関与する。近年、シングルセル解析技術の進展により、TAMの分子的多様性と極性転換の実態が明らかになりつつあるが、その上流でTAMの機能を制御する腫瘍由来因子、とりわけ糖タンパク質を介した免疫調節メカニズムについては未解明の部分が多く残されていた。
がんに高発現する糖タンパク質「GPNMB」に着目
研究グループは、がん細胞に高発現する糖タンパク質「GPNMB(Glycoprotein non-metastatic melanoma protein B)」に注目した。GPNMBは、乳がん、悪性黒色腫(メラノーマ)、脳腫瘍など多くの悪性腫瘍で過剰発現しており、がん幹細胞性や転移促進といった腫瘍悪性化に関与することが示唆されている。特に、トリプルネガティブ乳がん(TNBC:エストロゲン受容体、プロゲステロン受容体、HER2受容体がすべて陰性の乳がん)では、GPNMBは免疫抑制性TAMのマーカーとしても報告されているが、TAMの極性変換を誘導する「上流因子」としての役割や、シアル酸を介した免疫チェックポイント受容体Sialic acid-binding Ig-like lectin 9(Siglec-9)との関係性については、これまで明確にされていなかった。
そこで今回の研究では、GPNMBが高度に発現するTNBCにおいて、TAMと腫瘍の上皮間葉転換(epithelial-mesenchymal transition:EMT)を同時に誘導する分子機構の解明に取り組んだ。
TNBCにおいてGPNMBがSiglec-9と結合、TAMの自己増幅ループを形成
ヒト組織のRNA-seqやレクチン解析(糖鎖構造解析)などから、GPNMBはTNBCで著しく高発現するとともに過剰なシアル酸修飾を受け、Siglec-9と協調的に発現して予後不良と関連することが示された。
さらに、腫瘍細胞由来GPNMBではα2,3-シアル化が主体である一方、マクロファージ由来GPNMBではα2,6-シアル化が主体であることが判明した。GPNMBとSiglec-9の結合はシアル酸修飾に依存しており、そのパターンの違いによってSiglec-9は腫瘍細胞由来GPNMBをより選択的に認識していた。
また、腫瘍細胞と単球の3次元共培養モデルを用いた解析により、腫瘍GPNMBが単球内のGPNMB発現を誘導し、免疫抑制的かつEMT関連のTAMへと分化させる「自己増幅ループ」が形成されることを確認した。この結果、腫瘍内には炎症性と免疫抑制性の両極性を持つTAMネットワークが構築され、転移促進に寄与することが示唆された。
Siglec-9+PD-1同時阻害により肺転移が著明に減少、併用療法の有効性をマウスで確認
マウスモデルを用いた免疫療法実験では、Siglec-E(マウスにおけるヒトSiglec-9の機能的相同分子)と免疫チェックポイント受容体PD-1を同時に阻害すると、IL-6を介したEMTを抑制し、肺転移の著明な減少をもたらした。この際、免疫抑制性TAMおよび抑制性T細胞(Treg)の抑制に顕著な効果が見られた。CD8+T細胞活性に関しては、PD-1単独阻害と比較して異なる作用プロファイルを示した。これにより、併用療法における有効性と作用機序の違いが明確になった。
GPNMB-Siglec-9軸がTNBC進行・治療抵抗性の中心経路、新規標的として期待
今回の研究により、腫瘍細胞に発現するGPNMBとマクロファージに発現するSiglec-9との相互作用による腫瘍微小環境の免疫抑制的な再プログラム化が、TNBCの進行と治療抵抗性に関与する中心的な経路であることが明らかになった。
「GPNMB-Siglec-9軸は、TNBCの新たな治療標的となる可能性がある」と、研究グループは述べている。
▼関連リンク
・筑波大学 TSUKUBA JOURNAL



