主流の自家神経移植術はしびれ・痛みが残る場合あり、人工神経では効果が得られず
京都大学は3月7日、末梢神経損傷に対する新しい治療法としてバイオ3Dプリンタを用いた神経再生技術を開発し、世界で初めて患者に移植する治験「末梢神経損傷を対象とした三次元神経導管移植による安全性と有効性を検討する医師主導治験」を実施したと発表した。この研究は、同大医学部附属病院整形外科の松田秀一教授、同大医学部附属病院リハビリテーション科の池口良輔准教授ら、株式会社サイフューズの秋枝静香代表取締役らの研究グループによるもの。研究成果は、「Communications Medicine」にオンライン掲載されている。
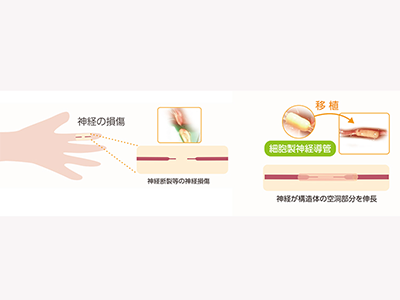
画像はリリースより
(詳細は▼関連リンクからご確認ください)
現在の末梢神経損傷治療は、患者自身の健常な神経の一部を採取して神経損傷部に移植する「自家神経移植術」が主流だ。この神経を採取する部分には、しびれや痛みが残ることから、患者にとって必ずしも最適な治療方法ではない。そのため、世界中で人工物を用いた神経再生技術の開発が行われている。しかし、これまで開発されてきた人工神経では自家神経移植術を超える結果は得られず、安全性においても課題を残していた。
バイオ3Dプリンタで細胞のみから三次元神経導管を作製、基礎研究で効果を確認
これまでに、佐賀大学の中山功一教授、株式会社サイフューズが開発したバイオ3Dプリンタを用いて細胞のみから成る三次元神経導管の作製に成功し、池口良輔准教授はラットの坐骨神経損傷モデルおよびイヌの尺骨神経損傷モデルに移植する基礎研究を行ってきた。この結果、自家神経移植に遜色なく、安全性においても問題のない結果を得ることができた。このメカニズムとして、線維芽細胞から作製した三次元神経導管からのサイトカイン放出や、三次元神経導管内部の毛細血管形成によって、軸索が良好に再生したと考えられた。
患者3人の皮膚由来線維芽細胞から三次元神経導管を製造・移植、12か月観察
これらの基礎検討を経て、京都大学医学部附属病院の医薬品等臨床研究審査委員会(治験審査委員会)の承認を得て、医薬品医療機器総合機構(PMDA)に治験計画届を提出し、2020年11月より「末梢神経損傷を対象とした三次元神経導管移植による安全性と有効性を検討する医師主導治験」を開始した(jRCT2053200022)。治験参加への同意を得られた患者自身から、腹部の皮膚の一部を提供してもらい、京都大学医学部附属病院C-RACT内の細胞調製施設(CCMT)において、患者の皮膚から線維芽細胞を分離、培養。この線維芽細胞を、株式会社サイフューズの開発した臨床用バイオ3Dプリンタを用いて三次元神経導管を製造した。
今回の治験では3人の患者の皮膚由来の線維芽細胞から三次元神経導管を製造して患者自身の神経損傷部位に移植し、移植後12か月まで観察を行った。
患者3人全員で知覚神経の回復・機能的な回復、安全性も確認
その結果、3人の患者全てにおいて知覚神経の回復・機能的な回復を認め、現職へ復帰することができた。また、すべての患者に副作用や問題になる合併症の発生はなく、三次元神経導管移植の安全性および有効性を確認できた。
今後、再生医療等製品の承認取得・社会実装を目指す
末梢神経再生の開発については、これまで京都大学と株式会社サイフューズが日本医療研究開発機構(AMED)等の公的機関の支援のもと、研究開発から臨床開発までを進めてきた。その後、実用化に向けた製品開発については株式会社サイフューズ主導のもと、太陽ホールディングス株式会社をはじめとする連携企業等の共同開発パートナーとともに将来の商業生産体制構築に向けて、開発を進めてきた。今般、医師主導治験の良好な結果発表と治験成果の論文化という開発成果を達成したことにより、今後は、株式会社サイフューズと太陽ホールディングス株式会社および太陽ホールディングス株式会社の子会社で医療品の開発製造受託事業を行う太陽ファルマテック株式会社(太陽HDグループ)が主導する形で、新たな再生医療等製品の上市および新たな再生医療の社会実装という産官学連携の実現に向けた活動を加速させていくという。同大は株式会社サイフューズと太陽HDグループと2019年の業務資本提携以来、同三次元神経導管の臨床開発と並行して、将来の再生医療等製品の事業化へ向けて共同で検討を進めてきた。2021年には、医師主導治験の実施と並行して商業化へ向けた企業間提携を強化し、太陽ファルマテック株式会社は、高槻工場内にコンパクトかつシームレスな細胞加工施設を竣工させた。同施設は、今般の治験成果と業務提携の進展を踏まえて、次相臨床試験以降の製造や同製品の商業生産施設として稼働する予定だ。
今後は、同三次元神経導管について再生医療等製品としての製造販売承認取得、社会実装を目指し、引き続き開発を進めていく予定。同製品の社会実装が達成されることで、外傷により神経損傷を受けた患者へ四肢の機能を再生・回復させる新たな治療選択肢として大きなQOL向上が見込まれる、と研究グループは述べている。
▼関連リンク
・京都大学 プレスリリース



