年間2兆円と言われる世界市場規模の胃酸抑制剤、新たな構造を持つ薬剤が求められている
名古屋大学は9月29日、AI、有機化学、構造生物学を活用し、胃酸抑制剤の候補となる新しい化合物の創生に成功したと発表した。この研究は、同大細胞生理学研究センターの阿部一啓准教授、大学院創薬科学研究科の横島聡教授、株式会社理論創薬研究所の吉森篤史博士、株式会社インテージヘルスケアらの研究グループによるもの。研究成果は、「Communications Biology」にオンライン掲載されている。
画像はリリースより
(詳細は▼関連リンクからご確認ください)
食物消化時に分泌される胃酸によって、ヒトの胃の内部は強い酸性(pH1)になる。胃の表面は粘膜によって保護されているため傷つくことはまれであるが、暴飲暴食や肉体的精神的ストレスによって粘膜が減少したり、ピロリ菌の感染によって粘膜が損なわれたりすると、胃酸は自分自身を傷つけてしまう。これが不快な胸焼けや、ひどい場合には胃潰瘍や逆流性食道炎と言われる症状の原因である。この治療のためには、胃酸の出る元を閉じればよいが、この胃酸の出る元、強い酸性の原因である水素イオン(H+)を出しているのが、胃の表面に存在する「胃プロトンポンプ」と呼ばれるタンパク質である。
この「胃プロトンポンプ」の働きを阻害する薬剤は、胃酸抑制剤と呼ばれ、オメプラゾールに代表される「プロトンポンプインヒビター(PPI)」や、ボノプラザンに代表される新しいクラスの薬剤「K+拮抗型アシッドブロッカー(P-CAB)」が実際の治療に使われている。これらの薬剤はまた、胃がんの主原因とされるピロリ菌を除菌する際に、抗生物質の効き目を担保するために胃酸を中和する目的でも使用される。このほかにもさまざまな用途で使用され、その世界市場の規模は年間2兆円とも言われている。より迅速で確実な治癒のために、また効き目の個人差を減らすため、未知の副作用や他の薬物との相互作用を回避するために、既存の薬剤とは大きく異なる化学構造を持った薬剤を開発することは、治療の選択肢を広げることにつながる。
ユニークな構造の胃酸抑制剤化合物デザインにAIを活用
研究グループは、これまでに複数の胃酸抑制剤が胃プロトンポンプに結合した状態を、X線や電子顕微鏡を使って調べることで、既存の薬剤や阻害剤がタンパク質のどの部分に結合しているかという情報を得ていた。これらの薬剤は全てH+の通り道に結合して、これを塞ぐことで酸を「ブロック」する。しかし、化合物によって結合する場所が少しずつ違っている。例えばP-CABのプロトタイプ化合物として知られるSCH28080はXとYの2か所で結合しているが、vonoprazanはXとYとは異なる領域Zを介して結合している。研究グループは、その場所(X、Y、Z)全部に結合できる新しい化合物があれば、より強く結合できるのではないか、と考えた。
しかし、結合する場所にちょうどいい具合に結合できる化合物を考えるのは簡単ではない。これまでは、既存の薬剤/阻害剤の構造を参考に、官能基を加えたり変更したりして、より高い親和性のものを作り出すという方法が行われてきた。しかしこの方法では、化合物の骨格に起因する副作用や薬物動態の大幅な改善は望めず、良いものが得られた場合でも特許によってその化合物が利用できないことがある。
そこで、既存の化合物とは全く異なるユニークな構造の化合物をデザインするためにAIを活用した。研究グループは、機械学習を応用してde novo化合物をデザインできるソフトウェア「Deep Quartet(DQ:ディープカルテット)」を開発してきた。今回の研究ではこの方法を使って、胃プロトンポンプ構造の任意の場所に結合部位(ファーマコフォアフィーチャー)を複数指定し、これをつなぐ化合物をデザインした。
100以上の候補化合物の中から、基準となる化合物より強く結合するDQ-06を発見
DQによってデザインされた百数十の候補の中から、有機化学、構造生物学の観点から適していると考えられるもの(指定したファーマコフォアとの一致具合、化学合成の難易度、想定される側鎖との相互作用、合成可能な化合物であること、など)を選び出し、実際に化合物を合成、胃プロトンポンプの活性阻害を指標として、その化合物の親和性(どれくらい強く結合するか)を調べた。すると6番目に合成した化合物(DQ-06)が、基準となる化合物(SCH28080)よりも強く結合することがわかった。
DQ-06と結合ポケットの隙間を確認、塩素原子を導入したDQ-18を合成し改良に成功
研究グループは、DQ-06が実際にはどのように胃プロトンポンプに結合しているのかを明らかにするため、クライオ電子顕微鏡を使って、化合物の結合状態を「視る」ことにした。大型放射光施設SPring8に設置された共用電子顕微鏡によって2.08オングストロームという高分解能で化合物を視ることに成功した。その結果、化合物が想定通りに結合していることが確認された一方で、化合物と結合ポケットの間には隙間があることを見つけた。
この隙間を埋めることで、化合物がよりぴったりとポケットに収まり、強く結合するはずであると考え、DQ-06に塩素原子(Cl)を1つ導入した、少し大きめの新しい化合物DQ-18を合成した。予想通り、DQ-18はポケットに隙間なくぴったりとはまり、結合力も強くなった。
さまざまなドラッグターゲットへの応用が期待できる「AI×化学×電子顕微鏡」の枠組み
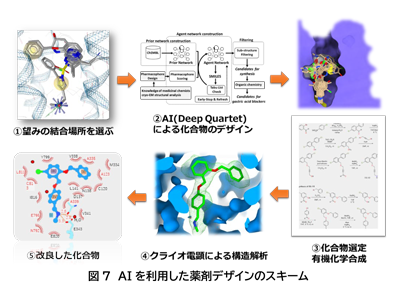
このように、1)既存のタンパク質構造から薬剤の結合に重要な部分を選び出す、2)結合に重要な部分を満たす新規化合物をAIによってデザインする、3)化学的な視点から適切なものを選び出し化学合成する、4)化合物の結合構造をクライオ電子顕微鏡で見る、5)さらに改良を加える、というステップを経ることで、胃酸抑制剤のプロトタイプ化合物であるSCH28080と比べて10倍近く親和性の高い化合物を創製することに成功した。
AIを活用したドラッグデザインの中でも、今回の報告は、難易度の高い膜タンパク質を対象として、AIによりデザインされた化合物を実際に合成し、その結合状態を実験的にクライオ電子顕微鏡で決定、さらに構造情報に基づいた化合物の改良を達成した初めての例である。「この枠組み(AI×化学×電子顕微鏡)は、胃プロトンポンプに対する胃酸抑制剤だけでなく、創薬ターゲットの半分以上を占めると言われる多くの膜タンパク質を含む、他のさまざまなドラッグターゲットへの応用が期待される」と、研究グループは述べている。
▼関連リンク
・名古屋大学 研究成果発信サイト



