肝障害時の肝星細胞活性化と細胞間線維化促進メカニズムに着目
東邦大学は6月23日、肝線維化を進行させる新たな細胞間ネットワークを発見したと発表した。今回の研究は、同大医学部生化学講座の関崇生助教、医学部生体防御研究室の中野裕康特任教授(同大研究統括機構副機構長)、薬学部の土屋勇一准教授、国立国際医療研究センター研究所の田中稔室長らの研究グループによるもの。研究成果は、「iScience」に掲載されている。
画像はリリースより
(詳細は▼関連リンクからご確認ください)
肝星細胞は、肝臓の類洞と肝細胞の間(Disse腔)に位置する間葉系由来の細胞である。健康な状態では、肝星細胞は静かにビタミンAを蓄える役割を担っているが、肝臓が傷つくと一変する。活性化されて筋線維芽細胞のような形になり、線維性の物質(コラーゲンなど)を大量に産生して肝臓を”硬くする”役割を担ってしまう。研究グループは今回、こうした肝星細胞が、どのように互いに影響を及ぼしながら線維化を広げていくのかを明らかにした。
活性化肝星細胞が産生するOPN、静止期細胞を選択的に活性化し正の連鎖反応形成
研究グループはまず、新鮮に単離した肝星細胞をFGF18、または線維化を誘導することで有名なサイトカインであるTGFβで刺激し、1細胞RNAシークエンス解析を実施した。共通して発現が増加する遺伝子の中から、組織修復や線維化に関与するSpp1(オステオポンチン:OPNの遺伝子名)に注目した。
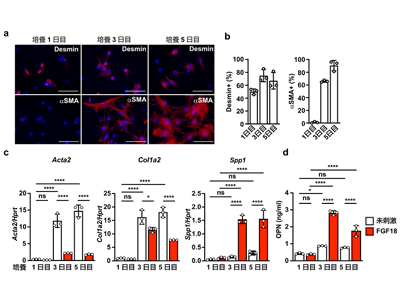
解析の結果、活性化状態の肝星細胞では、FGF18によるOPNの発現が大幅に増加することが判明し、さらにTGFβはFGF18によるOPNの発現をさらに増強する効果があることが認められた。また、OPNは静止期の肝星細胞に線維化遺伝子を誘導する一方、すでに活性化した細胞には作用しないことが明らかになった。このことから、活性化肝星細胞が分泌するOPNが、周囲の静止期肝星細胞を選択的に活性化させ、正のフィードフォワードループを形成することが示唆された。
肝線維化モデルマウスで検証、OPN/FGF18介した肝星細胞へのシグナル伝達を確認
生体内の検証では、肝線維化モデルマウスにおいて、OPNがαSMA陽性の活性化肝星細胞/筋線維芽細胞に局在し、Desmin陽性の静止期肝星細胞には発現しないことが免疫染色で確認された。さらに、脂肪性肝炎モデルマウスの1細胞RNAシークエンスデータを再解析した結果、筋線維芽細胞がOPNとFGF18を高発現し、OPNはインテグリン受容体を介して、FGF18はFGFR1/2を介して肝星細胞にシグナルを伝達していることが明らかになった。
肝線維化の新たな分子ネットワークモデル提唱、治療標的としても期待
研究グループは今回の研究結果をもとに新たなモデルを提唱した。肝細胞死によってTGFβが放出され、それがFGF18の産生を誘導し、FGF18が肝星細胞の増殖と活性化を促進し、OPNを産生する。OPNが静止期の肝星細胞をさらに活性化させるという、肝線維化を進行させる新たな分子ネットワークモデルである。
「単なる1つの因子の作用ではなく、細胞同士の連携と環境の変化が複雑に関与するダイナミックな現象として肝線維化を捉える視点を提供する。このFGF18-OPN経路は治療標的としても期待される」と、研究グループは述べている。
▼関連リンク
・東邦大学 プレスリリース



