mtDNA標的の遺伝子編集、ミトコンドリアの二重膜構造により困難とされてきた
北海道大学は6月20日、ミトコンドリア標的型ナノカプセル(MITO-Porter)を用いてCRISPR/Cas9ゲノム編集装置(RNP)を哺乳類細胞のミトコンドリア内に直接送達し、特定の遺伝子変異を標的としたミトコンドリアDNA(mtDNA)のゲノム編集に成功したと発表した。今回の研究は、同大大学院薬学研究院の山田勇磨教授、薬学研究院修士課程の野呂田楓氏(研究当時)、リューベック大学(ドイツ)の廣瀬みさ主任研究者らの研究グループによるもの。研究成果は、「Scientific Reports」にオンライン掲載されている。
画像はリリースより
(詳細は▼関連リンクからご確認ください)
ミトコンドリアは細胞のエネルギー産生を担う極めて重要な細胞小器官であり、細胞の生存や機能維持に不可欠なATPを産生する。加えて、独自の遺伝子(mtDNA)を有しており、核DNAとは異なる独立した遺伝情報を保持している。mtDNAの変異は、ミトコンドリア病をはじめとするさまざまな難治性疾患を引き起こし、現在でも有効な治療法が限られている。しかしながら、ミトコンドリアは二重膜構造を有し、外来分子の取り込みが極めて難しいため、これまでmtDNAを標的とした遺伝子編集は技術的に大きな課題となっていた。
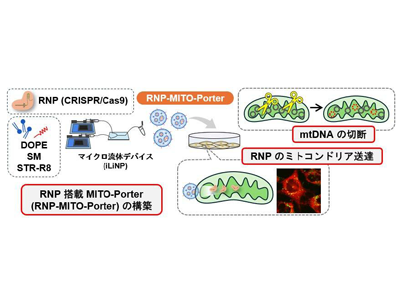
ミトコンドリアを標的にゲノム編集装置を送達するRNP-MITO-Porter構築
研究グループはこの壁を突破するため、MITO-Porterに着目し、ゲノム編集装置であるRNPを効率的かつ直接的にミトコンドリア内へ送達する技術の開発に挑戦した。これまでに、MITO-Porterを開発してミトコンドリアを標的とする薬物送達療法の検証を進め、さらに北海道大学大学院工学研究院の渡慶次学教授、真栄城正寿准教授と連携し、マイクロ流体デバイス技術を用いることにより、ナノレベルで精密に設計されたMITO-Porterの製造を実現していた。今回の研究ではこの技術を生かし、RNPを搭載したRNP-MITO-Porterの構築を行った。
マウス由来m.7778G>T変異細胞で特異的な二本鎖切断に成功、ヒト細胞でも同様の結果
まず、m.7778G>T変異を持つマウス由来のミトコンドリア変異細胞を用いて、特定変異部位に対するゲノム編集能力を詳細に評価した。さらに、一般的なヒト細胞(HeLa細胞)にも同様のアプローチを適用し、技術の汎用性と再現性を検証した。
単離ミトコンドリアにおけるRNP-MITO-Porterの活性評価において、MITO-Porterへの内包によってRNPのDNAの二本鎖切断活性が損なわれないことが示された。また、MITO-Porterを介してミトコンドリア内に送達されたCRISPR/Cas9複合体は、ターゲットとするmtDNA配列を特異的に認識し、効果的な二本鎖切断を誘導した。特に、m.7778G>T変異を有するマウス由来細胞においてゲノム編集の可能性が示唆され、さらにヒト細胞においても同様の結果が得られた。
ミトコンドリア機能障害に起因する幅広い病態への応用にも期待
今回の研究成果は、これまで困難とされてきたミトコンドリアへのゲノム編集装置の直接送達を実現したものであり、ミトコンドリア遺伝子疾患治療に向けた画期的な基盤技術となると考えられる。
この成果により、ミトコンドリア遺伝子疾患に対して、従来の対症療法ではなく、根本的な原因に直接アプローチする治療戦略の可能性が大きく拓かれた。さらに同技術は、ミトコンドリア病に限らず、他の難治性疾患や加齢関連疾患など、ミトコンドリア機能障害に起因する幅広い病態への応用も期待されている。「今後、他種ミトコンドリア変異モデル細胞や動物個体を用いた応用研究を推進し、臨床応用に向けた開発を加速させていく予定である」と、研究グループは述べている。
▼関連リンク
・北海道大学 プレスリリース



