EGFRと物理的に結合し安定化させるSTAP-2、結合領域の解析で阻害するペプチドを探索
北海道大学は11月28日、種々の上皮系がん細胞の増殖を制御する細胞内タンパク質であるSignal-transducing adaptor protein-2(STAP-2)のアミノ酸配列を鋳型にした2D5阻害ペプチドを同定したと発表した。この研究は、同大大学院薬学研究院の鍛代悠一助教、松田正教授らの研究グループによるもの。研究成果は、「The Journal of Biological Chemistry」に掲載されている。
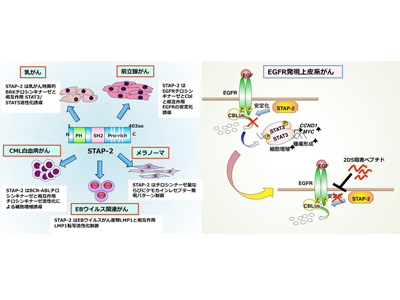
画像はリリースより
(詳細は▼関連リンクからご確認ください)
がんは日本の死因の第1位であり、より有効な治療薬の開発が望まれている。近年ではがん細胞に多く存在する特定のタンパク質に作用する薬剤(分子標的薬)によるがん治療が行われ、その有効性と安全性が注目されている。通常、細胞の増殖や機能分化は、細胞間で情報を伝達する「信号分子」と呼ばれる分子の緻密な相互作用のもとに成り立っている。細胞の増殖や機能分化メカニズムの異常は、細胞のがん化につながり、転移や腫瘍形成など、がんの悪化にも信号分子の異常が深く関わっている。特に上皮がんの増殖には、がん細胞を増殖させるスイッチの役割を果たすタンパク質の、EGFRの関与が知られている。EGFRはがん細胞の表面に多く存在し、このEGFRを構成する遺伝子の一部(チロシンキナーゼ部位)が変異すると、がん細胞を増殖させるスイッチが常にオンとなっている状態になり、がん細胞が限りなく増殖してしまう。EGFRは、細胞膜を貫通する状態で存在しており、細胞表面のEGFRに細胞の増殖を誘導する情報伝達物質のEGF等が結合すると、活性化したEGFRは細胞内に向けて増殖命令の信号を送る。これが細胞内の核に伝えられ、がん細胞は増殖する。
研究グループは、過去にSTAP-2とEGFRの関係を検討し、STAP-2はEGFRと物理的に結合することと、STAP-2が結合することでEGFRタンパク質の分解が抑えられ、EGFRが安定化することを解明した。つまり、STAP-2発現低下ヒトがん細胞では細胞表面のEGFRのタンパク量が減少するため、EGFの働きがうまく伝わらず、細胞増殖の低下が観察されたことがわかった。今回の研究ではSTAP-2とEGFRとの結合領域を解析。両者の結合を阻害するSTAP-2由来阻害ペプチドを検索し、最適化を行い、それを利用してがん細胞の細胞増殖や生体内腫瘍形成、EGFRの信号伝達においてどのように働くかを検討した。
STAP-2とEGFR相互作用領域の解析から設計した合成ペプチドに、細胞膜透過性を付加
STAP-2とEGFR間の相互作用を、STAP-2の3つの機能ドメインPH、SH2並びにC末ドメインをそれぞれ欠損させた欠損変異体(ΔPH、ΔSH2、ΔC)、あるいは機能ドメイン体のみと同時にグルタチオン−S−トランフェラーゼ(GST)にEGFRの細胞内ドメインのみを結合させたGST-EGFR細胞内領域融合タンパク質を作成し、両者発現ベクターをヒト胎生腎がん細胞株293Tに発現させることで、グルタチオンーセファロースによる沈降反応により、相互作用を解析した。その後、同定した相互作用領域のアミノ酸配列に対する20-30残基合成ペプチドを設計した。その際、細胞膜透過性向上には塩基性アミノ酸であるアルギニンの複数個付与が有効なので、設計した配列のN末端にオクタアルギニン(R8)とグリシンを付加した細胞膜透過性ペプチドを作製した。次いで、これらの合成ペプチドを用いて前立腺がん細胞株DU145の細胞増殖への影響を解析することで、増殖抑制効果の強い配列を有するペプチドを選別、最適化した。最適化した2D5阻害ペプチドを用いて、種々のヒトがん種への効果、細胞膜透過性配列R8の効果、ウエスタンブロット法や免疫沈降法を用いてEGFRとの結合への影響、EGR下流信号伝達への影響、EGFR依存性への影響、さらにEGFRタンパク質量への影響を解析した。最後に、細胞株接種マウスに2D5阻害ペプチドを投与した際の腫瘍形成を解析した。
STAP-2由来7アミノ酸の2D5ペプチド、種々のEGFR発現上皮系がん細胞の増殖を抑制
グルタチオンーセファロースによる沈降反応によるSTAP-2とEGFR間の相互作用の解析により、PHドメインのみでGST-EGFR細胞内領域融合タンパク質と結合することが明らかとなった。そのため、STAP-2PHドメインに対する合成ペプチド(20-30アミノ酸残基)を設計し、これらペプチドのN末端には膜透過性を付与するオクタアルギニン配列(R8)を付加した。これら合成ペプチドを用いてヒト前立腺がん細胞株を用いた細胞増殖測定を行い、がん細胞増殖抑制効果がみられる1種において最適化を行い、STAP-2由来7アミノ酸の2D5ペプチドを同定した。
2D5ペプチドのがん細胞増殖抑制活性にはR8による膜透過性が必須であり、2D5ペプチドはEGFR発現を示すヒト前立腺がん、肺がん、乳がんなど種々の上皮系がんに対してがん細胞増殖抑制活性を示した。さらに2D5ペプチドはSTAP-2とEGFRとの相互作用も抑制し、EGF刺激によるEGFR下流シグナル伝達、ERKや転写因子STAT3活性化や下流遺伝子発現に対しても抑制効果を示した。また、これらの効果はEGFR発現のない大腸がん細胞株SW620やEGFRノックダウンDU145細胞株においては観察されなかった。2D5ペプチドはSTAP-2によるEGFRタンパク質安定化にも抑制的に働き、2D5ペプチド処理により、EGFRのリソソームへの集積とタンパク質分解が促進された。さらに、ヒト前立腺癌腫細胞株DU145やヒト肺癌細胞株A549での免疫不全ヌードマウスにおける腫瘍形成は2D5ペプチド投与で抑制された。一方、EGFR発現のない大腸がん細胞株SW620でのヌードマウスにおける腫瘍形成は2D5ペプチド投与による効果は認められず、STAP-2由来2D5ペプチドはEGFR依存的なシグナル阻害により、がん増殖を抑制することが明らかとなった。
有機合成や化学修飾が可能な点でも優れるペプチド
今回の研究により、新規STAP-2由来2D5ペプチドのがん細胞増殖抑制効果を明らかにした。ペプチド創薬は、新規創薬において重要なターゲット領域として注目されている。特にペプチドはその細胞膜の透過性、安定性、結合力の観点で優れているだけでなく、それらの機能を向上させるための有機合成や化学修飾が可能なことから、従来の分子標的医薬品に代用される新規創薬として期待されている。「今後、STAP-2由来2D5ペプチドのさらなる最適化や化学修飾により、新規がん治療薬の開発が進むことが期待される」と、研究グループは述べている。
▼関連リンク
・北海道大学 プレスリリース



