なぜPol III欠損が脳の髄鞘形成不全を起こすのか?
国立精神・神経医療研究センター(NCNP)は10月16日、小児の遺伝性神経難病である先天性大脳白質形成不全症の1つ、Pol III関連白質変性症(Pol III-associated leukodystrophies)の新たな病態メカニズムを見出したと発表した。この研究は、NCNP神経研究所疾病研究第2部の李コウ研究員、井上健室長らの研究グループが、浜松医科大学医化学講座の才津浩智教授、神奈川県立こども医療センター遺伝科の黒澤健司部長、熊本再春医療センターとの共同研究として行ったもの。研究成果は、「Neurology Genetics」に掲載されている。
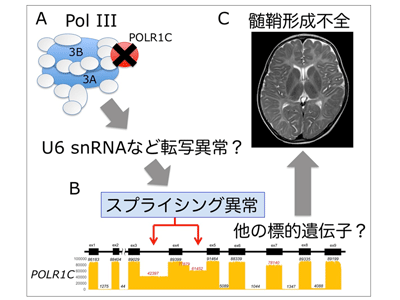
画像はリリースより
頭部MRI画像検査で典型的な髄鞘形成不全を呈する所見を示す症例の中には、特異的診断をつけることが困難である症例が少なからずある。これらの症例の中から、NCNP小児神経科の佐々木征行部長らは2009年、髄鞘形成不全に小脳萎縮と脳梁低形成を合わせもつ一群を新たな疾患として報告した。類似の疾患は、同時期に他の研究者からも報告されており、それらの異同が論議されていたが、2011年に原因遺伝子としてPol III複合体の主要な構成タンパク質であるPOLR3AおよびPOLR3Bをコードする遺伝子の変異がこれらの疾患の原因として同定され、Pol III関連白質変性症として疾患概念が確立された。さらに2015年に同複合体の構成タンパク質の1つをコードするPOLR1C遺伝子の変異も同定された。近年、これら3つの遺伝子変異をもつPol III関連白質変性症の症例の報告が増えており、臨床像の多様性も明らかになってきた。
Pol IIIは、トランスファーRNA(tRNA)、5SリボゾームRNA(rRNA)、U6核内低分子RNA(snRNA)など小さなRNAの転写を担うRNAポリメラーゼで、生体内のほぼすべての細胞に発現され、細胞機能の根幹となる作用を担っているが、なぜその機能の欠損が脳の髄鞘形成不全という特異的な現象を起こすのか、その分子病態については全く解明されていない。
POLR1Cの変異によるスプライシング制御異常が発症の一端を担う可能性
今回の研究は、2016年に熊本再春医療センターからの1例の患者の診断に関する相談から始まった。井上室長らは以前より「PMDと類縁疾患に関するネットワーク」というウェブサイトを通じて、診断に難渋している先天性大脳白質形成不全症の患者に関する診断コンサルテーションを研究班として実施しており、本症例もここで相談を受けた。患者の脳MRIでは、広範な髄鞘化不全を認めたため、原因不明の先天性大脳白質形成不全症と考え、メンデル遺伝病パネルエクソーム解析を実施したところ、POLR1C遺伝子に疾患の原因と思われる変異を発見。正常とは異なるアミノ酸配列に変化させる2つの変異は、それぞれ両親から1つずつ引き継いでおり、複合ヘテロ接合体であることが確認された。
さらにこれらの変異がどのようにPOLR1Cタンパク質の機能障害を引き起こすのかを検証するために、培養細胞や患者の末梢血細胞を用いてPOLR1C遺伝子およびタンパク質の発現解析を実施。その結果、それぞれ1か所のアミノ酸の変異をもつPOLR1Cタンパク質は細胞内での分布が異常になることがわかったが、それ以外にスプライシング異常によりイントロン部分を含む異常なPOLR1CメッセンジャーRNA(mRNA)が存在することがわかった。このスプライシングの異常を詳細に検討するために、近年可能になったロングリードシーケンシングを用いた全長のPOLR1C mRNA解析を実施。その結果、患者では85%以上の転写産物にスプライシング異常があることが判明した。また、健常な保因者である両親でも同様の解析を行ったところ、両親ともに同様のスプライシング異常を認めた。さらに驚いたことにこのスプライシング異常は変異を持たない正常のPOLR1C遺伝子アレルにも生じていることが判明した。
もしPOLR1C変異が自身のスプライシング異常を直接引き起こしていると仮定すると、両親での変異のないPOLR1C遺伝子アレルにスプライシング異常が存在することを説明できない。むしろ、変異によってPol IIIタンパク質の機能が損なわれた結果、本来PolIIタンパク質によって正常に転写されるはずのRNAに異常をきたし、その影響がPOLR1C遺伝子自身を含む標的遺伝子のスプライシング制御に異常をもたらしたと考えられる。これらの結果から、Pol IIIの生理的機能の1つとして、U6snRNAなどの標的RNAの転写調節を介してさまざまな遺伝子のスプライシングを制御していると考えられた。そして、その構成要因であるPOLR1Cの変異によってスプライシング制御の異常をきたすことがPol III関連白質変性症を引き起こしている可能性が示唆された。これまでPol III関連白質変性症の病態機序は全くわかっていなかったが、今回の研究によりスプライシング制御の異常がその一端を担っていると推測された。
今回の研究結果は、Pol III関連白質変性症の病態解明の第一歩となると考えられるが、同疾患の理解と克服のためには、まだ解明しなければならない課題が数多く存在する。具体的には、髄鞘形成を担うオリゴデンドロサイトでどのような遺伝子がPol IIIによるスプライシング制御を受けているのかを明らかにする必要がある。研究グループでは今後、POLR1C遺伝子変異を持つ患者の血液細胞由来のiPS細胞を樹立し、これを用いた解析を進めることで、今回明らかになったスプライシング異常が髄鞘化の障害を引き起こすメカニズムを解き明かすことを目指しているという。またPOLR1C以外のPol III関連白質変性症の原因遺伝子(POLR3AおよびPOLR3B)でも共通した病態が存在するのか、解析を進めていく予定だとしている。「これらの病態メカニズムを明らかにすることで、本疾患の治療標的分子を明らかにし、今後の治療につなげることができると期待される」と、研究グループは述べている。
▼関連リンク
・国立精神・神経医療研究センター トピックス



