さまざまながん種で確認されるIL-34、TNBCとの関連は?
北海道大学は7月22日、予後不良な乳がんとして知られるトリプルネガティブ乳がん(TNBC)において、がん細胞が分泌するインターロイキン-34(IL-34)そのものが予後不良に寄与していることを明らかにしたと発表した。これは、同大遺伝子病制御研究所病態研究部門免疫生物分野の清野研一郎教授、大塚亮助教、同大学院医学院修士課程の梶原ナビール氏らの研究グループによるもの。研究成果は、「Breast Cancer」オンライン版に掲載されている。
画像はリリースより
乳がんは、がん細胞の表面に出ている受容体の種類によって大きく4つのタイプに分かれる。TNBCは、乳がんの治療標的となる3つの受容体が欠如していることから、そのように名付けられており、全乳がんの約20%を占める。他のタイプの乳がんと比較して、より高い再発率、再発後の急速な進行を示し、予後が不良だ。TNBCに対する薬剤治療としては、抗がん剤を用いた化学療法が一般的だが、多くの患者が化学療法への抵抗性を獲得してしまうため、化学療法に取って代わるような効果的な治療法・治療薬の開発が強く望まれている。
マクロファージは、免疫のさまざまな側面で重要な役割を担っている一方、腫瘍に浸潤しているマクロファージの多くは免疫抑制性に偏っている。腫瘍におけるマクロファージによる免疫抑制を解除することが、がん治療法の1つとして注目を浴びており、世界中で数多くの研究が行われている。マクロファージを免疫抑制性に変える因子として、「IL-34」が報告されている。研究グループはこれまでに、さまざまながん種の腫瘍組織においてIL-34の発現を確認しており、がん細胞から産生されるIL-34が、がんの悪性度に関わることや、がんの進行を促進することを明らかにしてきた。しかし、TNBCにおけるIL-34の役割についての報告は未だない。そこで今回の研究では、TNBCの腫瘍組織におけるIL-34の発現と、TNBCの病因と予後におけるIL-34の役割、さらに、IL-34がTNBCにおいて治療標的となり得るかを検討した。
他の乳がんタイプよりもTNBC患者でIL-34高発現
まず、1,083人の乳がん患者の臨床情報をもとに、全乳がん患者を4つのタイプ別(TNBC、HER2+、Luminal A、Luminal B)に分類し、各タイプの乳がん組織におけるIL-34の遺伝子発現を比較。また、その発現が各タイプの乳がん患者の予後に影響するかを調べた。次に、IL-34を発現するマウスTNBC細胞株である4T1細胞を用いて、IL-34のTNBCにおける役割について検討。IL-34を欠損させた4T1細胞を樹立し、IL-34の有無で細胞の増殖能に差があるのかを調べた。さらに、IL-34の免疫系への作用を評価するため、IL-34を発現する細胞と欠損させた細胞を実験用マウスの皮下に注入し、生体内での腫瘍形成能と免疫細胞への影響を評価。最後に、マウス生体内で増殖した各腫瘍内に浸潤している免疫細胞の種類や量を解析することで、がん細胞から産生されるIL-34がTNBCの腫瘍環境にどのような影響を与えるのかを検証した。
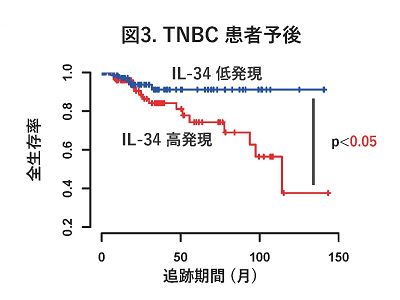
各タイプの乳がんにおけるIL-34の遺伝子発現を解析したところ、TNBC患者の腫瘍組織でのみIL-34が高発現していることが判明。また、TNBC患者171人のうちIL-34高発現患者と低発現患者に分けて生存率を解析したところ、IL-34高発現患者の生存率が、低発現患者に比べ有意に低くなることが確認された。さらに、IL-34そのものが独立した予後不良因子であることを突きとめた。つまり、IL-34の発現は、他のタイプの乳がんよりもTNBCで高く、IL-34の高発現が単独でTNBC患者の予後不良因子となることを明らかにした。また、マウスTNBC細胞株を用いた実験により、IL-34を発現する4T1細胞とIL-34を欠損させた4T1細胞の増殖能は、試験管内では差が無かったのに対し、実験用マウスの生体内では、IL-34を欠損させた4T1細胞の増殖速度が、IL-34を発現する4T1細胞と比較して、有意に遅くなることがわかった。
TNBC細胞が産生するIL-34がマクロファージの性質を免疫抑制性に変えている
この結果を踏まえ、研究グループはそのメカニズムを検討した。IL-34には免疫を抑制する機能が知られているため、IL-34を発現する4T1細胞でできた腫瘍と、IL-34を欠損させた4T1細胞でできた腫瘍に浸潤している免疫細胞の種類や量を解析。その結果、免疫細胞の種類や、各免疫細胞の浸潤率に差は認められなかった。一方、腫瘍環境における炎症がIL-34を欠損させた4T1細胞でできた腫瘍内で強まっていることがわかった。さらに、それらの炎症を引き起こしているのはマクロファージから産生された炎症性サイトカインであると判明。マクロファージ由来の炎症性サイトカインは、活性マクロファージで増加し、免疫抑制性マクロファージで減少することが知られている。このことから、TNBC細胞が産生するIL-34がマクロファージの性質を免疫抑制性に変えることで、腫瘍内に免疫抑制環境を構築し、腫瘍の成長を促進していると考えられる。
今回の研究により、TNBCにおいてIL-34が独立した予後不良因子であることが示された。IL-34を標的とした治療は、TNBC患者の予後を改善する可能性がある。「研究開発の推進により、TNBC局所におけるIL-34の発現診断→IL-34阻害薬の投与、という新しいがん個別化治療のパラダイムが生まれる可能性がある。今後IL-34阻害薬の開発が進み、臨床応用されることが期待される」と、研究グループは述べている。
▼関連リンク
・北海道大学 プレスリリース



