膵臓がん細胞のみで効果を発揮する治療薬を探索
名古屋大学は3月2日、タンパク質に翻訳されないRNA(長鎖非翻訳RNA)のうち、TUG1を標的とした治療薬が膵臓がんに対して有効である可能性を発見したと発表した。この研究は、同大大学院医学系研究科・腫瘍生物学分野の近藤豊教授、田﨑慶彦大学院生らの研究グループと、名古屋市立大学、東京大学、ナノ医療イノベーションセンター、がん研究会との共同研究グループによるもの。研究成果は、「Cancer Research」に掲載されている。
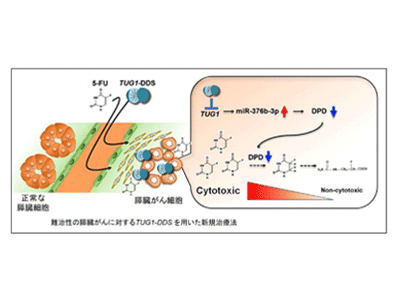
画像はリリースより
膵臓がんは、5年生存率が10%以下とがんの中で最も予後が悪い難治性のがんのひとつで、有効な治療法の開発は喫緊の課題と考えられている。手術による腫瘍の切除は、膵臓がんの重要な治療方法だが、診断がついた段階で手術できる患者は約20%に過ぎず、切除できても術後の再発率が高く、術後の5年生存率は20~40%と不良だ。そのため、ほとんどの膵臓がん患者に対して5-FUやゲムシタビンなどの抗がん剤による薬物治療を行うが、いまだに効果は限られている。
また、現在使用されている抗がん剤には「がん細胞が抗がん剤に対する耐性を獲得することにより効果を失ってしまう」「抗がん剤が正常細胞に毒性を示してしまう」という2つの課題がある。そこで研究グループは、膵臓がん細胞が抗がん剤耐性を獲得するメカニズムを解明し、膵臓がん細胞のみで効果を発揮する治療薬を見つけることを目的として研究を行った。
作製したUG1-DDSと5-FUの同時投与で5-FUの効果が増強し、マウスの膵臓がんが縮小
正常な膵臓細胞と膵臓がん細胞の遺伝子発現プロファイルを解析した結果、膵臓がん細胞でTUG1の発現が顕著に上昇していることがわかった。長鎖非翻訳RNAは、タンパク質に翻訳されないRNAの一種である小分子RNAと相互作用して、その小分子RNAの標的遺伝子の発現をコントロールする。そこで、TUG1と相互作用する可能性のある小分子RNAとその標的遺伝子を探索したところ、TUG1はmiR-376b-3pとの相互作用を介して、ジヒドロピリミジン脱水素酵素(DPD)の発現を増加させていることがわかった。DPDは5-FUを分解し、抗がん剤としての効果を減弱させる酵素として知られているが、TUG1はDPDの発現上昇を介して、膵臓がん細胞の5-FUの耐性獲得に寄与することを証明した。
次に研究グループは、TUG1の作用を抑制する薬剤の作製を試みた。薬剤をがん細胞のみに到達させるための「運び屋」と、TUG1を抑制する核酸医薬と組み合わせた治療薬(TUG1-DDS)を、ナノ医療イノベーションセンター、東京大学との共同研究で作製。このTUG1-DDSを用いることにより、TUG1の作用を抑制する薬剤を膵臓がん細胞のみに送達することができた。
さらに5-FUに耐性を示す膵臓がん細胞を移植したマウスにTUG1-DDSと5-FUを投与し治療効果を確認した結果、5-FUを単独で投与したマウスと比較して、TUG1-DDSと5-FUを同時に投与した場合では、5-FUの薬効が保たれ、顕著に腫瘍増殖が抑制したという。
TUG1-DDSは正常細胞への毒性を抑えつつ、膵臓がん細胞特異的に5-FUの効果を増強
今回の研究で、TUG1は膵臓がん細胞においてmiR-376b-3pとの相互作用を介してDPDの発現を上昇させることにより、5-FUの耐性を獲得する能力をもたらすことが世界で初めて明らかにされた。
「TUG1-DDSは膵臓がん細胞のみに送達され、効率的に5-FUの効果を増強するため、5-FUの投与量が少なくて済むことにより正常細胞への毒性を抑えつつ、難治性のがんである膵臓がんにおいて有効な治療薬となる可能性を見出すことができた」と、研究グループは述べている。
▼関連リンク
・名古屋大学 プレスリリース



