全身炎症を抑制する治療では予後改善せず、根本的治療法は未確立
横浜市立大学は11月14日、敗血症の病態解明と根本的治療法の開発を目的に研究を行った結果、コクサッキーアデノウイルス受容体(Coxsackievirus and adenovirus receptor:CXADR)が敗血症の原因物資であるエンドトキシンによる心不全(心機能障害およびショック)を制御し、さらにその機序としてCXADRが炎症惹起分子であるp38/p65の活性を制御することを明らかにしたと発表した。この研究は、同大医学部救急医学 西井基継講師、松村怜生助教らの研究グループによるもの。研究成果は、「Journal of Molecular and Cellular Cardiology Plus」に掲載されている。
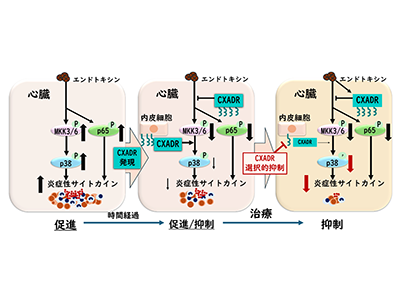
画像はリリースより
(詳細は▼関連リンクからご確認ください)
敗血症は、感染症などを契機とした全身炎症疾患であり、特に心不全を代表とした臓器障害やショックを合併した場合は、致死的な経過をたどることが知られている。したがって、新型コロナウイルス感染症に代表される感染症パンデミックの際に、敗血症は大きな社会問題となる。
これまで、全身炎症を抑制する治療法が試みられてきたが、予後の改善には至らず、いまだに根本的治療法が確立されていないのが現状である。このことは臓器局所炎症の重要性を示唆しているが、その制御機序は十分に解明されていない。
ストレス時の臓器炎症に関わるCXADRに着目、敗血症制御への関与を検証
CXADRは、元来ウイルス受容体として発見されたが、その後の研究により、細胞接着分子として作用することが明らかになった。特にストレス時の臓器恒常性や臓器炎症において、重要な役割を果たしている。
そこで研究グループは「CXADRは敗血症臓器障害の重要な制御分子である」という仮説を立てた。
CXADRが「炎症促進」と「炎症抑制」という二重の役割を持つことを発見
研究では、全身あるいは内皮細胞選択的にCXADR遺伝子を欠損させたマウスにエンドトキシンを全身投与し、生体内でのCXADRの役割を検討した。その結果、CXADRはエンドトキシンによる不全心臓において発現が亢進し、炎症促進および炎症抑制の二重の役割を果たしていることが示された。さらに内皮細胞特異的欠損では、全身欠損とは対照的に主な炎症惹起分子であるp38の活性が抑制された。
CXADRが、心不全やショックを伴った重症敗血症の治療標的分子候補となる可能性
今回の研究により、細胞起源に応じたCXADRによる多様なp38活性制御は、敗血症に伴う局所臓器炎症の新たな制御機序であり、特に血管内皮細胞に発現するCXADRは、心不全やショックを伴った重症敗血症の新たな治療標的分子の候補となることが示された。
「敗血症は病態異質性が大きい疾患であり、他の敗血症モデルでの検討を行っていく。さらにsiRNAなど核酸医薬の血管内投与により、敗血症臓器障害出現後における血管内皮CXADR発現制御の治療効果を検証する。これらの結果に基づいて、創薬開発を進めていく」と、研究グループは述べている。
▼関連リンク
・横浜市立大学 プレスリリース



