父方由来遺伝子に起因する遺伝性疾患、従来は対症療法のみ
慶應義塾大学は10月29日、エピゲノム編集技術によりプラダー・ウィリー症候群(Prader-Willi syndrome:PWS)の失われた遺伝子の働きを回復させる方法を開発したと発表した。この研究は、同大再生医療リサーチセンター、医学部臨床遺伝学センター、東京医科大学小児科・思春期科学分野の共同研究グループによるもの。研究成果は、「Nature Communications」に掲載されている。
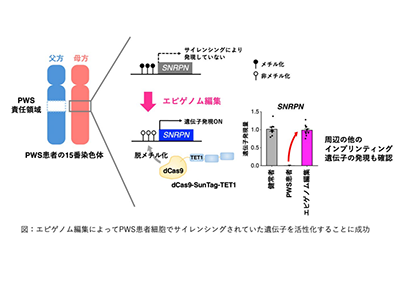
画像はリリースより
(詳細は▼関連リンクからご確認ください)
PWSは、染色体15番の特定領域にある父方由来遺伝子の働きが失われることで発症する。出生直後から筋力低下や発達遅滞が見られ、成長とともに強い食欲、肥満、ホルモン異常など多彩な症状を呈する。原因は視床下部の機能不全と考えられているが、根本的な治療法は存在せず、従来は対症療法に限られていた。
患者は母方染色体上に同じ遺伝子を保持しているものの、エピゲノムにより発現が抑制されている。この「サイレンス化」を解除し、母方遺伝子を再活性化できれば、病態の改善につながる可能性がある。過去には薬剤によるエピゲノム改変が試みられたが、効果が限定的で副作用の懸念もあった。そのため、特定遺伝子を精密に制御できるCRISPRベースのエピゲノム編集が注目されている。
エピゲノム編集で母方遺伝子を再活性化、オルガノイドで有効性・安全性を確認
今回の研究では、PWS患者由来のiPS細胞を用い、「CRISPR/dCas9-Suntag-TET1システム」という最新のエピゲノム編集技術を適用した。まず、DNAのメチル化を取り除くことで、母方の染色体上の遺伝子を再活性化した。この母方遺伝子の再活性化により、広範な「サイレンス化」が解除されていることを網羅的なエピゲノム解析で可視化した。
次に、視床下部オルガノイドにおいても、サイレンス化の解除および遺伝子機能の回復が持続することを確認した。この結果から、エピゲノム編集によって回復させた遺伝子の働きがオルガノイドに分化させた後も持続することが示され、臨床応用に近い環境での有効性が明らかになった。
さらに、シングルセル解析により、PWS特有の異常な遺伝子発現パターンの回復を確認した。標的外でのメチル化改変は確認されなかったことから、安全性の観点からも有望であることが示唆された。
PWSの新たな治療戦略、他のインプリンティング疾患への応用にも期待
今回の研究により、世界で初めて「ヒト視床下部モデルにおいて、エピゲノム編集でPWS関連遺伝子を回復できる」ことが示された。この成果は、あくまで細胞やオルガノイドを用いた基礎研究段階のものだが、エピゲノム編集技術は薬剤による脱メチル化治療と比べて選択性が高く、長期的な効果が期待できるため、今後さまざまな領域への展開が見込まれる。
「本研究は、PWSに対する根本的治療法がなかった状況を打破し得る、分子レベルでの新しい治療戦略を提示するものだ。この成果は、他のインプリンティング疾患への応用可能性も示しており、今後の再生医療・遺伝子治療研究に大きな一歩をもたらすことが期待される」と、研究グループは述べている。
▼関連リンク
・慶應義塾大学 プレスリリース



