なぜ低酸素脳障害に痛風治療薬が効くのか?
東京大学は2月20日、痛風治療薬として使われているフェブキソスタットが脳を低酸素傷害から保護することを明らかにしたと発表した。この研究は、同大大学院農学生命科学研究科の岡本研特任研究員、佐藤奈々技術補佐員、永田宏次教授、日本医科大学の草野輝男助教らによる研究グループによるもの。研究成果は、「Brain Research」にオンライン掲載されている。
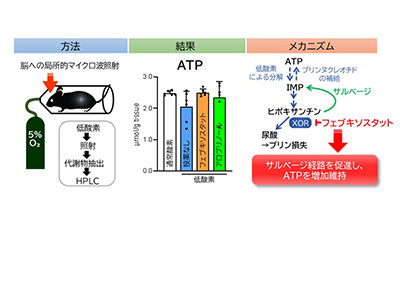
画像はリリースより
(詳細は▼関連リンクからご確認ください)
循環器不全や呼吸不全、低酸素環境などによって脳への酸素供給が滞ると、脳機能は速やかに傷害される。この脳損傷にはアデノシン三リン酸(ATP)の枯渇が関与している。
痛風治療薬であるアロプリノールは、低酸素脳傷害に対する保護効果があることが報告されていたが、その作用機序は明らかになっていなかった。また、別の痛風治療薬であるフェブキソスタットの脳保護作用については、十分に研究されていなかった。
そこで、今回の研究では、低酸素条件におかれたマウスの脳内ATPおよびその代謝物の濃度変化を測定することで、アロプリノールとフェブキソスタットの影響を検証した。
フェブキソスタットにアロプリノールよりも強いATP維持効果
研究グループは、低酸素を維持したままマイクロ波を照射することで脳の代謝を瞬時に停止させ、ATPおよびその代謝物を測定する手法を開発した。この手法により、従来は困難だった低酸素による脳内ATP代謝変化を正確に捉えることが可能になった。
5%の低酸素条件に3分間置かれたマウスの脳では、ATPレベルが低下し、ATP分解物であるAMPや尿酸が増加した。フェブキソスタットを投与したマウスでは、低酸素条件下でも高いATPレベルが維持され、AMPレベルも低いままだった。これらの結果は、フェブキソスタットが低酸素によるATP分解を軽減させたことを示している。
一方、アロプリノールを投与した場合には、フェブキソスタットほど顕著な効果は見られなかった。尿酸生成阻害効果については両薬剤に差がなかったことから、ATP維持効果のメカニズムには尿酸は直接関与していないことが示唆された。
痛風治療薬によるATP維持効果、考えうるメカニズム
ATPの分解物であるヒポキサンチンは、サルベージ経路によって再びプリンヌクレオチドへ戻り、ATP合成に寄与する。しかし、キサンチン酸化還元酵素(XOR)によってヒポキサンチンがキサンチン、さらに尿酸へと分解されると、サルベージされることなく、排泄される。
低酸素ストレスによってATP分解が進むと、ヒポキサンチンが増加する。ヒポキサンチンは血中に移動し、肝臓でXORによって尿酸へと変換される。プリン体は尿酸になってしまうと、もうATPへ戻ることができないため、体内のATP合成材料が減少していき、その結果、脳内のATP濃度も減少する。
フェブキソスタットはXORを阻害することで尿酸生成を抑制し、体内のヒポキサンチンを高める作用がある。XORが阻害されると、ヒポキサンチンは肝臓で尿酸に変化せず血中に放出され、脳に取り込まれると考えられる。脳はサルベージ経路が発達しているため、ヒポキサンチンをATPへ再合成する能力が高い。フェブキソスタットは、このメカニズムを介して、脳のATP維持に寄与している可能性がある。
アロプリノールもXOR阻害剤だが、アロプリノールはヒポキサンチンとよく似た化学構造であるため、サルベージ経路内の酵素を阻害することが知られている。この点が、今回の研究でフェブキソスタットとアロプリノールの効果に差が見られた原因と考えられる。
脳機能障害を低減する新たな治療法創出に期待
XOR阻害剤によってATPサルベージ経路を強化する戦略は、血流障害や呼吸障害による脳損傷の治療だけでなく、神経変性疾患やエネルギー枯渇に起因する疾患の治療法へ応用できる可能性がある。「今回の研究で用いた薬剤は既に医薬品として実績があり、安全性が確認されている。本剤を用いた新たな治療法が早期に生み出されることを期待する」と、研究グループは述べている。
▼関連リンク
・東京大学大学院農学生命科学研究科・農学部 研究成果



