さまざまなロドプシン遺伝子変異が原因、多様な異常形態により治療開発が困難
名古屋工業大学は9月19日、ロドプシンを特異的に認識する、ナノボディと呼ばれるラマ由来の特殊な抗体を発見し、ロドプシンにナノボディが結合した複合体の立体構造を、X線結晶構造解析により解明し、種々の分光計測手法および生化学的手法を組み合わせることで、ナノボディが、ロドプシンのミスフォールディングと過剰な光活性化を阻止できることを明らかにしたと発表した。この研究は、同大大学院工学研究科の渡辺航平氏(研究当時:工学専攻生命・応用化学系プログラム博士前期課程2年)、神取秀樹特別教授、片山耕大准教授、米国カリフォルニア大学アーバイン校のクリストフ・パルチェフスキー特別教授らの研究グループによるもの。研究成果は、「Nature Communications」に掲載されている。
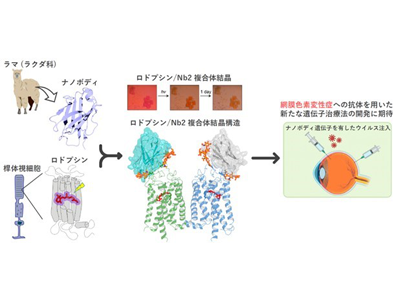
画像はリリースより
(詳細は▼関連リンクからご確認ください)
網膜色素変性症は、眼の奥の網膜に異常をきたす遺伝性かつ進行性の眼疾患群である。日本では4,000~8,000人に1人が発症すると推定されており、夜盲、視野狭窄、視力低下が特徴的な症状である。網膜の中には光受容細胞として知られる、桿体視細胞と錐体視細胞の2種類が存在し、それぞれ明暗視、色覚を担う。網膜色素変性症はこれら2種類の視細胞のうち桿体が主に障害されることによって引き起こされることが多く、暗いところで物が見えにくくなったり(夜盲)、視野が狭くなったりするような症状を最初に起こす。そして病気の進行とともに錐体も障害され、視力低下を自覚するようになる。現在、網膜色素変性症の根本的な治療法は確立されておらず、遺伝子治療や神経保護、細胞移植などの研究が世界中で盛んに行われている状況である。
ロドプシンは、桿体視細胞に含まれる、光受容機能の根源を担う分子であり、ロドプシンにおけるさまざまな遺伝子変異が原因で網膜色素変性を発症すると考えられている。網膜色素変性症の患者において、150以上のロドプシン遺伝子の変異が確認されており、これらロドプシン遺伝子の変異によってタンパク質のミスフォールディングや、光刺激に関係なく恒常的にロドプシンが活性化してしまう異常など、ロドプシン遺伝子の変異箇所の違いによって異常形態も多様化していることが、特定の標的遺伝子治療の開発を困難にしていると考えられている。
ロドプシンの光受容機能に重要な、活性化に至るまでの全ての分子機構は未解明
また、ロドプシンを標的とした創薬や遺伝子治療法の開発に向けては、ロドプシンの光受容機能を支える分子基盤を解明することが重要になる。ロドプシンはGタンパク質共役型受容体(GPCR)ファミリーに属するが、GPCRの中でも最初にX線の結晶構造が決定された分子で、種々の分光解析や機能解析、計算科学的解析など、機能発現の分子機構に関する研究が最も進んでいる分子であるが、その全容までは明らかにされていないのが現状である。例えば、ロドプシンによる視覚の機能発現において、光反応過程で生理的に重要と考えられているミリ秒から秒の時間領域では、メタロドプシンI(メタI)と活性中間体メタロドプシンII(メタII)がpH平衡の関係にあるが、立体構造が解明されているのはメタIIのみで(メタIに至るまでに生成する光反応中間体の構造は決定されている)、メタIIを形成するまでのタンパク質内部で起こる分子機構の理解は遅れている。活性化に至るまでの全ての構造が解明され、構造基盤に立脚した活性化の分子機構の理解が深まれば、ロドプシンの過剰な活性が原因で進行する、桿体視細胞の変性を阻止できる創薬および遺伝子治療の研究につながることが期待される。さらに、上述の通り、ロドプシンはGPCRの中で最も分子機構解明に向けた研究が進んでいる分子であることからも、GPCRの活性・不活性化を制御する新たな薬剤設計指針を提示できる可能性もある。
光活性化過程を停止し、メタI中間体の立体構造解析を可能にするナノボディ低分子抗体を同定
今回、研究グループは、ロドプシンの光活性化過程で生成する中間体のうち、いまだ立体構造が解明されていない、メタI中間体の高分解能構造決定に向けて、ロドプシンの光活性化過程を停止させ、メタI中間体の立体構造解析を可能にする、ナノボディとして知られる特殊なタイプのラマ由来抗体を獲得することに成功した。具体的には、ラマから産生した、ウシ由来のロドプシンを抗原とする30種類のナノボディ低分子抗体を、ELISA法(enzyme linked immunosorbent assay法)によって同定した後、光存在/非光存在の条件下において、共免疫沈降法、Blue-Nativeポリアクリルアミドゲル電気泳動法および表面プラズモン共鳴分光法を用いたロドプシンとナノボディとの結合親和性を評価する実験を通じて、最終的に、光存在下でのみ特異的かつ強固にロドプシンに結合する4種類のナノボディ低分子抗体を獲得することに成功した。
ナノボディ・ロドプシン複合体構造を高い分解能で解明することに成功
そこで、得られた4種類のナノボディとロドプシンを光存在下で混和させた後、X線結晶構造解析を試みることで、うち1種類のナノボディとロドプシンとの複合体(ロドプシン-ナノボディ複合体)の立体構造を3.7オングストローム(1オングストロームは100億分の1m)の分解能で解明することに成功した。得られたロドプシン-ナノボディ複合体は、二量体を形成していた。また、ナノボディはロドプシンの細胞外側の第2ループを含む表面領域を幅広く認識するように結合していた。特に、ナノボディ低分子抗体の超可変領域であるCDR1とCDR3がロドプシンの細胞外第2ループのアミノ酸と静電的かつ分子間相互作用を介して結合していることが明らかとなった。さらに、ナノボディのCDR1およびCDR3領域のアミノ酸変異実験により、ロドプシンとの結合に特に重要なアミノ酸を特定することにも成功した。
ナノボディ、レチナールシッフ塩基の加水分解反応阻害しロドプシン光活性化を阻害
次に、ロドプシン-ナノボディ複合体構造がどの中間体状態を取っているかを明らかにするため、紫外可視吸収分光および透過型赤外吸収分光計測手法を用いた解析を行い、ロドプシン-ナノボディ複合体がルミ/メタI様の中間体であることを明らかにした。つまり、期待通り、獲得したナノボディはロドプシンの光活性化を阻害し、活性前駆体を構造的に安定化することがわかった。さらに研究グループは、ナノボディがどのようなメカニズムでロドプシンの活性化を阻害しているのかを明らかにするため、蛍光分光計測手法と液体クロマトグラフィー質量分析法を組み合わせた解析を行うことで、ナノボディの結合によって、ロドプシン内部に結合したレチナールシッフ塩基の加水分解反応が阻害されていることを明らかにした。一般に、ロドプシンは光を吸収する前の始状態において、レチナールシッフ塩基は正電荷を帯びており、近傍に存在する負電荷を帯びたグルタミン酸との静電相互作用によって安定化されているが、光活性化時に、シッフ塩基のプロトンが脱離することで、細胞質側領域の構造変化を誘発する。その後、脱プロトン化したシッフ塩基は加水分解反応の影響を受け、ロドプシンのタンパク質内部からレチナールが解離する。今回、ナノボディが、ロドプシンの細胞外側第2ループに結合することで、レチナール結合部のタンパク質環境が安定化され、プロトンの脱離反応が抑制された結果、光活性化が阻害されたと解釈される。
ナノボディ、網膜色素変性症の原因となるロドプシンP23H変異体のミスフォールディングも阻害
また、研究グループは、ナノボディがロドプシンのミスフォールディングを阻害する役割も果たすのではないかと仮説を立てた。そこで、ロドプシンのミスフォールディングが原因で網膜色素変性症を引き起こすことが知られている、ロドプシンP23H(23番目のプロリン残基がヒスチジン残基に変異)変異体に対するナノボディの阻害効果を、免疫蛍光染色によるイメージングを用いて解析を行った。ロドプシンP23H変異体はタンパク質のフォールディング過程で異常が生じ、細胞膜まで正しく輸送されず小胞体に局在することで、桿体視細胞の変性につながり、最終的には網膜色素変性を発症すると考えられている。期待通り、ロドプシンP23H変異体とナノボディを共発現させた哺乳類細胞(HEK293細胞)では、野生型と同程度のロドプシンP23H変異体の細胞膜への発現が確認され、ナノボディがロドプシンP23H変異体のミスフォールディングを阻害したことで、正しく細胞膜へ輸送されたことを示した。以上の結果より、今回獲得したナノボディは、ロドプシンの光活性化のみならず、ミスフォールディングを阻害することが明らかになった。
ロドプシン活性化に至る分子機構の一端解明、網膜色素変性症の遺伝子治療につながると期待
今回、ロドプシンにおいて唯一立体構造が解明されていなかった、メタI中間体様の構造を決定したことで、活性化に至るまでの分子機構の一端が明らかになった。特に、従来、細胞外側におけるレチナールを結合させる部位の変化は、続く光反応過程で情報伝達に重要な細胞質側領域に伝わることが知られていたが、今回の研究によって、細胞外側領域に存在する自由度の高いループ構造がアロステリックに細胞質側領域の大きな構造変化を制御していることが示唆された。これによって、GPCRを標的とした創薬研究に新たな設計指針を与えることが期待される。また、今回の研究対象であるナノボディ低分子抗体は、分子量が小さく、安定で可溶性であることから、通常の抗体が一般に接近できないエピトープ(抗原内で抗体が結合する部位)を認識でき、通常の抗体に代わる有望な抗体治療薬として注目されている。実際に、研究グループは、ナノボディ低分子抗体を遺伝学的に、網膜色素変性症モデル動物マウスに導入する研究を開始しており、桿体視細胞の細胞死抑制や視力改善について、評価をしていく予定である。「研究成果により、いまだ治療法が確立していない網膜色素変性症の遺伝子治療を可能にすることが期待される」と、研究グループは述べている。
▼関連リンク
・名古屋工業大学 プレスリリース



