自己免疫性胃炎と胃の神経内分泌腫瘍をつなぐメカニズムは未解明だった
大阪公立大学は9月26日、自己免疫性胃炎(autoimmune gastritis:AIG)から胃の神経内分泌腫瘍(neuroendocrine tumor:NET)発症に至るメカニズムの一端を明らかにしたと発表した。この研究は、同大大学院医学研究科消化器内科学の大谷恒史講師らの研究グループと米国Harvard大学の国際共同研究によるもの。研究成果は、「Journal of Gastroenterology」のオンライン版に掲載されている。
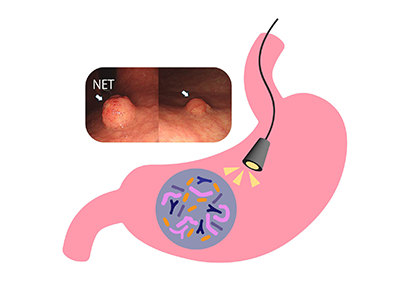
画像はリリースより
(詳細は▼関連リンクからご確認ください)
AIGは、自己抗体を介した免疫学的機序によって胃酸を分泌する胃壁細胞が破壊されることで起こる疾患である。AIGを発症すると、胃酸が分泌されなくなり(無酸症)、血中のガストリンが増加する。その結果、胃にNETという特殊な腫瘍ができやすくなる。
日本の健診受診者におけるAIGの有病率は0.49%程度と報告されており、AIGにおける胃NETの発生率は0.7~15.4%の範囲とされている。AIGはこれまでヘリコバクター・ピロリ胃炎の陰に隠れ、あまり注目されてこなかった希少疾患だが、近年AIGの診断基準や内視鏡所見が徐々に明らかにされ、この疾患への関心と注目が高まってきている。
通常、胃は強い酸性環境下にあるため、胃酸を中和する酵素(ウレアーゼ)をもつピロリ菌以外の細菌の生存は困難と考えられてきたが、解析技術の進歩により、実際には多様な細菌が胃に存在することが明らかになっている。AIGでは無酸症に伴う胃細菌叢のバランスの崩れ(ディスバイオシス)が確認されており、ピロリ菌による胃炎とは異なる細菌叢の特徴を示すことが報告されている。しかし、AIGにおける胃細菌叢の変化と胃NET発症の関連について、詳細なメカニズムは解明されていなかった。
そこで今回の研究では、胃粘膜に存在する細菌叢と組織内の代謝物質の両面から解析を行い、AIGにおける胃細菌叢の変化と胃NET発症の関連を明らかにすることを目的とした。
AIG患者の胃粘膜組織を解析、NET陽性群に特徴的な細菌叢パターン判明
2020年10月~2023年2月に同大医学部附属病院(旧:大阪市立大学医学部附属病院)で、AIGと診断された19人と健常対照者12人の胃粘膜生検組織を対象に、解析を行った。AIGの診断は、抗壁細胞抗体または抗内因子抗体の陽性、内視鏡で確認される胃体部の広範な萎縮、24時間インピーダンスpHモニタリングによる無酸症を基準とした。
まず、採取した胃粘膜検体からDNAを抽出し、16S rRNA遺伝子(V3-V4領域)の増幅産物を次世代シーケンサーで解析した。その結果、AIGでは胃細菌叢のα多様性(集団内における多様性を表す指標)が低下していた。β多様性(異なる集団間での多様性の違いを表す指標)については、対照群、NET陰性群、NET陽性群の間で、それぞれ異なる細菌叢の構成がみられた。特に、NET陽性群ではHaemophilus parainfluenzaeやFusobacterium属(F. periodonticum、F. nucleatum)が増加する一方、健康維持に関与する乳酸菌やStreptococcus salivariusが減少していた。さらに、胃細菌叢の相対存在量をヒートマップ解析した結果、NET陽性群では、対照群・NET陰性群と異なる構成パターンが認められた。
AIGでの代謝変化が胃NETに関わる細菌の増殖を促す可能性が明らかに
次に、キャピラリー電気泳動飛行時間型質量分析による組織内代謝物質の網羅的測定を行った。その結果、AIGでは解糖系やTCA回路の活性が低下し、代謝が代替経路へ切り替わる代謝リプログラミングが認められた。さらに、胃細菌叢と代謝物質を類似性に基づいて分類し、両カテゴリー間の関連性を「アリュービアルダイアグラム」で統合解析した結果、AIGと関連する組織代謝型と、胃NETに関連する胃細菌叢シグネチャーの特定に成功した。
これらの結果から、AIGでは宿主の代謝変化に続いて粘膜ディスバイオシスが生じ、胃NET形成に関わる特定の細菌が増加する微小環境が形成される可能性が明らかになった。
胃NETの早期発見・予防につながる研究成果、新たな診断指標の開発に期待
今回の研究により、AIGから胃NETが発症するメカニズムの一端が、宿主の代謝異常とそれに伴う細菌叢の変化によって説明できる可能性が示された。これらの知見は、AIGから胃NET発症に至る病態の理解を深め、胃NETの早期発見や予防につながる新しい診断指標の開発に役立つことが期待される。
「今後はより多くのAIG症例を対象に研究を進め、細菌叢や代謝の観点からAIGの病態解明をさらに進める予定だ」と、研究グループは述べている。
▼関連リンク
・大阪公立大学 プレスリリース



