胎盤が成熟する過程で、どのようにCYP19A1遺伝子のスイッチが入るのか?
藤田医科大学は5月14日、女性ホルモンである「エストロゲン」が胎盤で作られる仕組みを解明したと発表した。この研究は、同大医学部生化学の石原悟講師らのグループによるもの。研究成果は、「Endocrinology」に掲載されている。
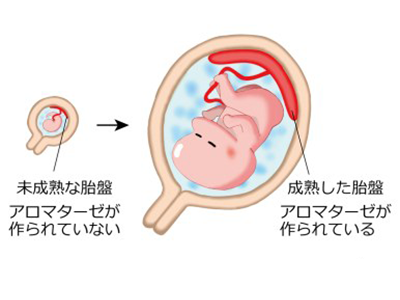
画像はリリースより
(詳細は▼関連リンクからご確認ください)
ヒトの転写因子の設計図は個々人の遺伝子に書き込まれており、それぞれのRNAを経て各転写因子が作り出される。また、アロマターゼなどの酵素もタンパク質の一種で、アロマターゼの遺伝子であるCYP19A1をコピーしたRNAを経てアロマターゼが作り出される。
アロマターゼが女性ホルモンであるエストロゲンを作る反応は、エストロゲンと構造が類似する男性ホルモンのアンドロゲンを作り変えることによって行われる。ヒトの胎児では、性別にかかわらず副腎という臓器で多量のアンドロゲンが作られる。そのため、アンドロゲンによる過度な男性化を防ぐために、過剰分のアンドロゲンを胎盤に運びアロマターゼの働きによってエストロゲンへ作り変えている。このように、アロマターゼが胎盤で働くことは妊娠時の重要な現象の一つであるにもかかわらず、胎盤が成熟する過程でどのようにCYP19A1遺伝子のスイッチが入るかについては、よくわかっていなかった。
そこで研究グループは今回、胎盤に見られる「AP-2γ」という転写因子に着目し、CYP19A1遺伝子のスイッチの制御を「3-デアザネプラノシン」で処理した胎盤の細胞を用いて検討した。
ヒト胎盤由来細胞<3-デアザネプラノシン添加培養<AP-2γ増加<CYP19A1遺伝子ON
ヒト胎盤由来の細胞株JEG3細胞を3-デアザネプラノシンのあり/なしで培養したところ、ありの場合にCYP19A1遺伝子のスイッチが入ることを発見した。同時にAP-2γの量が増えることを見出し、さらにAP-2γのCYP19A1遺伝子への結合が観察されたため、CYP19A1遺伝子のスイッチ・オンにAP-2γが関わることが明らかになった。
さらに観察すると、3-デアザネプラノシンを加えない培養条件下では、AP-2γの設計図が書き込まれているTFAP2C遺伝子のスイッチが入っているにもかかわらず、遺伝子からコピーされたRNAは微量しか検出できず、そのRNAにはメチル基が結合している状態であることが判明した。
胎盤でのエストロゲン産生、TFAP2CのRNAのエピジェネティック制御で調節の可能性
一方、3-デアザネプラノシンを加えた培養条件下では、メチル基が結合していないTFAP2C遺伝子のRNAが多量に観察された。このRNA量がAP-2γのタンパク質量の増加に反映され、その結果、CYP19A1遺伝子のスイッチが入れられて最終的にアロマターゼが作られることが明らかになった。両培養条件の比較から、TFAP2CのRNAに結合したメチル基がRNA自身の分解促進に働いたと解釈される。
これらの結果から、妊娠時の胎盤におけるエストロゲン産生が、TFAP2CのRNAが分解される/されないの調節で行われる可能性が考えられる。
3-デアザネプラノシンが胎盤成熟に役立つ可能性
同結果は、培養細胞を用いた基礎研究での成果であり、これがすぐに臨床応用できるわけではない。しかし、この研究成果と同様の現象が臨床試料において観察された場合、近い将来、3-デアザネプラノシンまたは類似する薬剤が、胎盤成熟に問題が見られる疾病に応用される可能性がある、と研究グループは述べている。
▼関連リンク
・藤田医科大学 プレスリリース



