逃避行動を調節するニューロンの神経活動は不明点が多かった
京都大学は6月14日、ショウジョウバエ幼虫の逃避行動をモデルにゲノムワイド関連解析(GWAS)を行い、痛みによる逃避行動を抑制する遺伝子を発見し、「belly roll(bero)遺伝子」と名付けたと発表した。この研究は、同大生命科学研究科の李愷(LI, Kai)研究員、司悠真博士課程学生、上村匡教授、碓井理夫講師らの研究グループによるもの。研究成果は、「eLife」オンライン掲載されている。
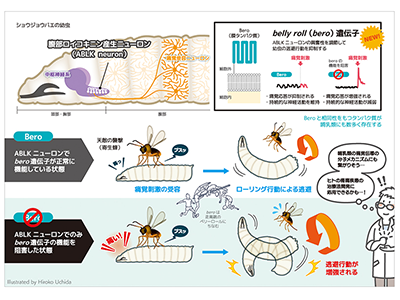
画像はリリースより
(詳細は▼関連リンクからご確認ください)
動物は生息環境に潜む危険を感知し、逃避行動により生存をはかる。特に、捕食者による襲撃を察知して逃避行動を取ることは、個体の生存に直結する重要な本能行動だ。モデル動物であるショウジョウバエ幼虫も、寄生蜂による産卵管刺入を痛覚刺激として感知し、体をよじって逃避することが知られている。さらに、寄生蜂の羽音を聞くと逃避行動が迅速化する。この行動迅速化は個体の生存に有利なため、逃避行動の調節は個体の生存にとって重要な生物機能だと言える。
逃避行動を制御する神経回路についてはこれまで、神経回路マップ解析による回路同定が進んできた。しかし、中枢神経系において痛覚入力情報を調節して個体の逃避行動を制御する神経メカニズムの多くは不明だった。これは、逃避行動を司る神経回路の活動ダイナミクスがよくわかっていないこともその一因だ。マウスでは、最近になって痛覚信号の伝達や統合のメカニズムが徐々に明らかになりつつある。
しかし、逃避行動を調節するニューロンの神経活動の詳細は未解明の点が多くある。したがって、痛覚伝導ニューロンの神経活動を詳細に把握して、その制御メカニズムを理解することは重要な研究課題だ。
ショウジョウバエ幼虫の逃避行動をモデルにGWASを実施し責任遺伝子を同定
この目的を達成する第一歩として、逃避行動を調節する未同定の遺伝子を同定してGWASを実施し、さらにその生理機能を理解することが重要だ。そこで研究グループは、ショウジョウバエ野生型系統の大規模コレクション「Drosophila Genetic Reference Panel(DGRP)」を利用して、遺伝子同定を試みた。これらの野生型系統は非常に多様な遺伝的背景(遺伝子多型)を持つため、個々の遺伝子の発現量や生理機能が系統ごとに異なっていると期待される。
各野生型系統のゲノムDNA配列が既知のため、それぞれの系統について痛覚逃避行動の感度を計測することにより、どの遺伝子多型が逃避行動の制御に関わるかを推定できる。研究グループは、30個以上の遺伝子を関連候補遺伝子として推定した。遺伝子ノックアウトやニューロン特異的な遺伝子発現抑制を利用した2次的な検証実験から、CG9336遺伝子を責任遺伝子として同定し、belly roll(bero)遺伝子と命名した。
幼虫の痛覚応答を増強すると起こる逃避行動をbero遺伝子が抑制
次に、幼虫神経系でのbero遺伝子の発現パターンを調べたところ、複数のペプチド産生ニューロンで発現していることがわかった。それぞれのペプチド産生ニューロンについて、特異的な遺伝子発現操作が可能であることを利用して、ニューロン群特異的な発現抑制実験を行った。
その結果、腹部ロイコキニン産生(Abdominal leucokinin, ABLK)ニューロンで発現するbero遺伝子が、逃避行動を抑制することがわかった。そこで、ABLKニューロンの逃避行動における役割を調べるため、ABLKニューロン特異的に神経活動を誘導したところ、逃避行動が引き起こされることがわかった。これらの結果は、幼虫が痛覚刺激を受けた際のABLKニューロンの神経活動(痛覚応答)が増強した結果、逃避行動が引き起こされること、その活動の増強をbero遺伝子が抑制していることを示唆している。
Beroタンパク質の機能が何らかの環境ストレスで調節され、痛覚応答が制御される可能性
この可能性を検証するため、ABLKニューロンの痛覚応答を、正常個体とbero遺伝子機能阻害個体との間で比較することを試みた。その結果、bero機能阻害ABLKニューロンは、正常ニューロンに比べて大きな痛覚応答を示すことがわかった。しかし、ABLKニューロンは痛覚刺激がない状況でも、持続的な神経活動を示したという。一方、bero機能阻害下ではこの持続的な神経活動が有意に減弱していた。
この持続的な神経活動の生理的な意義は不明だが、痛覚応答に何らかの影響を与えていると考えられた。Beroタンパク質の機能が何らかの環境ストレスによって調節されることで、痛覚応答が制御されている可能性があるとしている。
痛みを制御する新規治療法の発見に期待
哺乳類の痛覚伝導回路にはさまざまな経路が知られており、またそれが飢餓状態などの体内環境要因により調節を受けることが知られている。しかし、個々の痛覚伝導ニューロンがどのようなメカニズムで情報統合を行っているのかはわかっていない。今回の研究成果により、ショウジョウバエ幼虫のABLKニューロンの興奮性を調節する仕組みの一端が明らかにされた。哺乳類にもBeroタンパク質のホモログが数多く存在するため、そのいずれかが痛覚伝導ニューロンの興奮性を調節している可能性があると考えられる。
「そのような機能的ホモログの分子機能を検証することで、哺乳類の痛覚伝導の分子メカニズムをより深く理解できる可能性がある。これにより、痛みを制御する新規治療法が見つかることが期待される」と、研究グループは述べている。
▼関連リンク
・京都大学 最新の研究成果を知る



