NASH症例で鉄過剰、肝線維化における作用機序は?
名古屋大学は1月20日、非アルコール性脂肪肝炎(NASH)において、細胞内鉄含量の多い常在性マクロファージ(クッパ-細胞)が肝線維化(硬化)の進行に重要であることを明らかにしたと発表した。これは、同大環境医学研究所/医学系研究科の菅波孝祥教授、田中都講師、金森耀平研究員を中心とする研究グループによるもの。研究成果は、国際科学誌「iScience」に掲載されている。
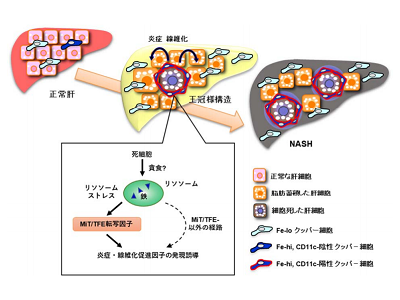
画像はリリースより
ライフスタイルの欧米化により、日本においてもメタボリックシンドロームの肝臓における合併症として、NASHが増加している。NASHは、予後良好の単純性脂肪肝とは異なり、炎症や線維化が慢性的に進行することで肝硬変や肝がんの発症につながること、現在有効な治療法がないことなどから注目されている。特に肝線維化は、肝硬変や肝がん、生命予後の規定因子として重要であり、NASHにおいて肝線維化を抑制する治療法の開発は喫緊の課題だ。日本における肝がんの主要な原因は、従来はウイルス性肝炎だったが、近い将来、NASHが取って代わると想定されている。
NASHの病態メカニズムとして「multiple parallel hits仮説」が提唱されており、過剰な脂肪蓄積やインスリン抵抗性などの代謝異常に、炎症性サイトカイン、酸化ストレスなどの炎症刺激が加わることでNASH発症に至るとされている。この炎症刺激の1つとして鉄代謝異常の関与が指摘されており、実際、NASH症例における鉄過剰が報告されているが、肝線維化における作用機序や肝臓内の責任細胞については十分にわかっていなかった。
研究グループはこれまでに、肝常在性マクロファージ(クッパー細胞)が肝細胞死に応答してCD11c陽性に形質転換し、炎症性サイトカインや線維化促進因子を産生して、脂肪肝からNASHに進展することを明らかにしている。
モデルマウスで、細胞内鉄含量の多いクッパー細胞が肝線維化の促進に働く
研究グループはまず、遺伝性肥満を呈するメラノコルチン4型受容体欠損(MC4R-KO)マウスを準備し、そのマウスに高脂肪・高ショ糖・高コレステロール食(ウェスタンダイエット)を負荷し、NASHを誘導。脂肪肝を発症したMC4R-KOマウスに鉄を投与したところ、肝線維化が増悪した一方、鉄を吸着するキレート剤の投与により肝線維化が抑制された。このことから、鉄はNASHにおける肝線維化の促進に働くことが明らかになった。また、MC4R-KOマウスに鉄を投与すると、鉄は主にクッパー細胞に蓄積し、CD11c陽性に形質転換した。
そこで、クッパー細胞と鉄代謝に注目して、詳細な解析を行った。正常肝、脂肪肝、NASH肝を呈するMC4RKOマウスの肝臓からクッパー細胞を調製。磁力を利用して細胞内鉄含量の多い(Fe-hi)クッパー細胞、少ない(Fe-lo)クッパー細胞に分離すると、病態の進行とともに、Fe-hiクッパー細胞が炎症・線維化促進因子(CD11c、TNFα、CCL3、TIMP1等)を高発現した。
ヒトNASHでもMiT/TFE転写因子の活性化が関わると推測
次に、クッパー細胞における鉄蓄積が、どのように形質転換をもたらすかを検討。NASH肝より単離したCD11c陽性クッパー細胞と鉄を負荷した培養マクロファージを用いて、マイクロアレイ解析により遺伝子発現プロフィールを網羅的に解析した。リソソーム機能調節に働くMiT/TFE転写因子に注目したところ、クッパー細胞に鉄を負荷すると、リソソーム機能が障害され、MiT/TFE転写因子のTFE3が活性化したことがわかった。クッパー細胞においてTFE3は、形質転換マーカーのCD11cや種々の炎症・線維化促進因子の遺伝子発現を誘導した。以上の結果から、NASHにおけるクッパー細胞の形質転換には、鉄蓄積によるMiT/TFE転写因子の活性化が関わっていると考えられた。
最後に、クッパー細胞におけるMiT/TFE転写因子の活性化が、NASHを発症したMC4R-KOマウスの肝臓において認められることを確認した。研究グループはこれまでに、CD11c陽性に形質転換したクッパー細胞が死細胞(肝細胞)を取り囲むように配置する特徴的な組織像(王冠様構造)を呈すること、ここを起点として炎症・線維化が進行することを報告している。今回、MiT/TFE転写因子は、王冠様構造を形成するクッパー細胞で活性化していることを明らかにした。また、研究グループは、MC4R-KOマウス以外のNASHモデルやヒトNASHにおいても、同様の所見を確認した。
今回の研究により、クッパー細胞は鉄含有量によって分類できること、鉄含有量の多いFe-hiクッパー細胞がNASHの発症過程において炎症・線維化促進的に働くこと、その分子メカニズムとしてMiT/TFE転写因子の活性化が重要であること、マウスNASHモデルのみならずヒトNASHにおいても同様のメカニズムが想定されることが明らかになった。「クッパー細胞に鉄が蓄積する機序、今回明らかになった経路を標的とする治療法の開発などが残された課題として挙げられる」と、研究グループは述べている。



