がん幹細胞
がんが生まれる元になっている細胞で、自己複製し永続的にがん細胞を作り続けるといわれているのが、がん幹細胞である。がん細胞の中で数%が、がん幹細胞といわれている。がん幹細胞は増殖が遅く、薬が効きにくい。 がん細胞を手術などで除去しても、がん幹細胞が体内に残っていると再発や転移が起きると考えられる。
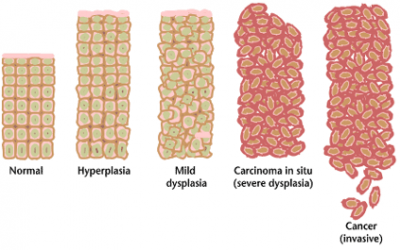
(画像はウィキメディアより)
がん幹細胞を阻害
大日本住友製薬は、開発中の抗がん剤「BBI608」に関する第1/2相試験のうち用量漸増試験の結果を発表した。本剤は、がん幹細胞の自己複製を阻害し、がん細胞に加え、がん幹細胞に対して細胞死を誘導する低分子化合物である。
本試験は、標準的治療で効果が得られなかった結腸直腸がん、頭頸部がん、胃がん、卵巣がん、メラノーマ、乳がんなど成人進行性がん患者41 例を対象とした、1 日1-3 回経口投与試験であった。患者を14 のコホートに分け、それぞれ1 日当たり、20 mg から2,000 mg までの14 段階で投与した。副作用の重篤度は、
グレード0:正常。
グレード1:無症状または軽症の症状がある。治療を要さない。
グレード2:中等症であり、最小限/局所的な治療を要する。
グレード3:重症または医学的に重大であるが、ただちに生命を脅かすものではない。入院または入院期間の延長を要する。
グレード4:生命を脅かす症状。緊急処置を要する。
グレード5:死亡。
グレード1:無症状または軽症の症状がある。治療を要さない。
グレード2:中等症であり、最小限/局所的な治療を要する。
グレード3:重症または医学的に重大であるが、ただちに生命を脅かすものではない。入院または入院期間の延長を要する。
グレード4:生命を脅かす症状。緊急処置を要する。
グレード5:死亡。
(大日本住友製薬のニュースリリースより引用)
その結果、最も多く見られた副作用は、グレード1~2 の下痢、吐き気、食欲不振、疲労であり、グレード3 は4 件(下痢及び疲労)、グレード4 はみられなかった。最大耐用量は確認されず、血液毒性も認められなかった。(堤朝子)
▼外部リンク
大日本住友製薬 ニュースリリース2013年6月4日
http://www.ds-pharma.co.jp/



