IBS発症における末梢SNSの関与は未解明だった
兵庫医科大学は10月28日、ストレスが腸の痛みを悪化させる仕組みを解明したと発表した。この研究は、同大解剖学神経科学部門の段韶琪助教、戴毅主任教授らの研究グループによるもの。研究成果は、「Cellular and Molecular Gastroenterology and Hepatology」に掲載されている。
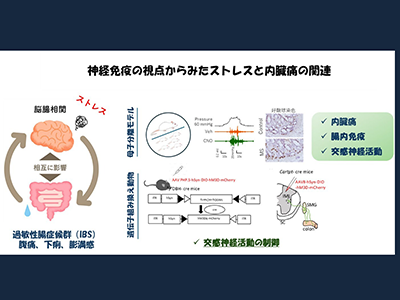
画像はリリースより
(詳細は▼関連リンクからご確認ください)
過敏性腸症候群(IBS)は、腹痛や下痢、便秘を繰り返す機能性消化管疾患であり、世界人口の約15%が罹患するとされている。器質的異常がみられないにもかかわらず、粘膜に軽度の炎症が存在し、肥満細胞や好酸球などの免疫細胞の浸潤が内臓痛と関連する可能性が報告されている。しかし、これらの免疫変化を引き起こす要因は明らかではなかった。
一方、心理社会的要因、特に幼少期のストレス経験は、成人期にIBSを発症するリスクを高めることが知られており、その際に交感神経系(SNS)の過敏化が生じることが報告されている。SNSはノルアドレナリンを介して免疫系に作用し、免疫応答を抑制または促進することが知られているが、IBSの発症における末梢SNSの関与は未解明だった。そこで今回の研究では、ストレスと腸管粘膜の免疫変容の関係、さらに内臓痛の発症との関連を明らかにすることを目的とした。
モデル動物で、活性化された交感神経が大腸粘膜に好酸球を集め炎症が起こることを確認
研究では、母子分離(maternal separation)ストレスモデルを用いて、交感神経過興奮が腸管免疫に及ぼす影響を解析した。さらに、化学遺伝学的手法により末梢SNSを選択的に制御し、交感神経の興奮が好酸球浸潤や内臓過敏に与える影響を検討した。
その結果、母子分離モデルにおいてIBSの特徴である腸の免疫異常と内臓痛を再現できることが確認された。ストレスを受けた動物では交感神経の働きが過剰となり、大腸粘膜に好酸球が集積した。交感神経活動を薬剤で抑制すると好酸球浸潤が減少し、痛みも軽減した。
交感神経の活性化で「エオタキシン-1」が放出され、腸の炎症・痛みを誘発
また、交感神経を化学遺伝学的手法で活性化させると、腸管粘膜の間葉系細胞を介して好酸球を誘引する物質「エオタキシン-1」が放出され、腸の炎症と痛みが誘発されることを確認した。さらに、IBS患者の大腸組織においてもエオタキシン-1の増加が認められた。
これらの結果から、ストレスによる交感神経の過剰な働きが腸の免疫異常と内臓痛を引き起こす一因であることが示され、新しい治療法の開発につながる可能性が示唆された。
神経-免疫連関を基盤とした機能性消化管障害の新規治療法開発に期待
今回の研究により、交感神経のシグナルが腸の間葉系細胞を介して、免疫応答や炎症に影響を及ぼす可能性が示された。「今後は、間葉系細胞が交感神経からの刺激をどのように受容し、炎症性サイトカインやケモカインを産生するのか、その分子メカニズムを詳細に解明することが課題だ。これらの知見は、神経-免疫連関を基盤とした機能性消化管障害に対する新規治療法の開発へとつながることが期待される」と、研究グループは述べている。
▼関連リンク
・兵庫医科大学 プレスリリース



