アドレナリン受容体阻害でK+の排出機構を促進、虚血後の脳損傷を軽減
理化学研究所は5月20日、マウスを用いた研究から、脳内のカリウムイオン(K+)の排出(クリアランス)機構を促進することにより、虚血後の脳損傷を軽減する仕組みを解明したと発表した。この研究は、同脳神経科学研究センター神経グリア回路研究チームの毛内拡客員研究員(お茶の水女子大学基幹研究院自然科学系助教)、平瀬肇チームリーダー、慶應義塾大学医学部の安井正人教授らの国際共同研究グループによるもの。研究成果は「Proceedings of the National Academy of Sciences (PNAS)」のオンライン版に掲載されている。
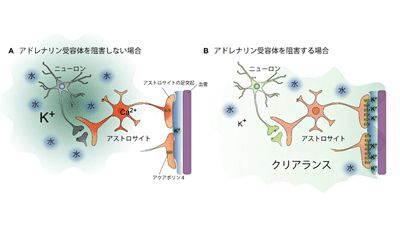
画像はリリースより
脳卒中や外傷性脳損傷などの脳血管障害では、多くの場合、障害発生部位のみならず健康な部位にまで損傷が拡大する二次的損傷が起こる。損傷拡大には、脳血管障害の最初期(超急性期)に繰り返し生じる異常な神経興奮の波の伝播(拡延性脱分極)が関与しており、その発生は、主に脳内のカリウムイオン(K+)濃度の急上昇が引き金となる。脳血管障害の一種である虚血性脳卒中では、脳血管が詰まること(梗塞)によって生じる虚血が組織の壊死を引き起こす。現在利用されている脳梗塞の治療法は、血栓溶解剤や脳保護薬などの対処療法であり、細胞外K+濃度の正常化を標的とした具体的な治療法の開発が喫緊の課題となっている。
頭蓋骨の中で脳が浸っている「脳脊髄液」には、Na+、K+等のさまざまなイオンが存在し、健常状態の脳では各イオン濃度は一定に保たれている。脳脊髄液は頭蓋内を循環し、その動態が脳機能の恒常性に重要な役割を果たしていると考えられるが、その詳細は完全には解明されていない。これまで脳脊髄液の動態に、水分子の動態が関与することに着目して研究を進めてきた研究グループは、脳脊髄液を脳組織内へ浸潤させる機序に、水分子の透過を担う「アクアポリン4」という膜タンパク質(チャネル分子)が関与することを既に報告した。
一方、アドレナリン受容体を阻害することによって、脳脊髄液の浸潤が促進されることが報告されていることから、脳脊髄液の動態に神経伝達物質のノルアドレナリンが関与している可能性が示されている。さらに脳梗塞の直後、脳のノルアドレナリン濃度が急激に増加することが知られている。これまで、脳梗塞の超急性期においてアドレナリン受容体に着目した研究結果は断片的に報告されているが、統一的な見解は得られてなかった。そこで研究グループは、アドレナリン受容体を阻害することで、脳脊髄液の浸潤を促進し、脳梗塞後の細胞外K+濃度の正常化を図れると予想した。
発生2時間以内であればアドレナリン受容体阻害薬の事後投与も有効
研究グループは、レーザーを用いた光血栓法によって、大脳皮質に局所的に脳梗塞を生じる脳梗塞モデルマウスを作製し、アドレナリン受容体阻害薬の効果を調べた。24時間後に脳の損傷を評価するTTC染色を行った結果、無処置マウスでは、レーザーを照射した面積よりも損傷部位が広がっていた。一方、アドレナリン受容体阻害薬をあらかじめ投与したマウスでは、損傷が最小限に食い止められていた。また、脳梗塞発生から2時間以内であれば、事後投与も有効だった。ヒトの脳梗塞に近いモデルとして用いられる、中大脳動脈閉塞・再灌流による脳梗塞モデルマウスでも同様の結果が得られたという。
また、右側大脳皮質に梗塞をおこしたマウスを透明な円柱の中で自由に行動させ、つかまり立ちをする際に使用する前肢の使用パターンを観察した(シリンダー試験)。その結果、マウスは脳梗塞後2日間にわたって、左側皮質が支配する右前肢を使用する頻度が上昇した。一方、アドレナリン受容体阻害薬投与マウスでは、左右の前肢の使用頻度に差は見られなかった。これにより、アドレナリン受容体阻害薬の事前投与は、行動試験による運動機能の回復にも有効であることがわかった。
アドレナリン受容体阻害でアクアポリン4の局在確保、K+排出で神経保護
次に、脳梗塞に伴う脳内の水の動きの変化を詳しく調べるために、主にアストロサイトに発現するアクアポリン4のみを蛍光物質で標識する手法(免疫組織化学染色法)を用いて、脳内のアクアポリン4の分布を可視化した。その結果、脳梗塞3時間後では、損傷部位でアクアポリン4の標識が約6割減少していた。アストロサイトにだけ発現している別のタンパク質(GLAST)は変化なく見られたことから、この減少が細胞死によるものではないと示された。その一方、アドレナリン受容体阻害薬を事前投与すると、アクアポリン4の標識が維持されることを見いだした。
さらに、アクアポリン4を欠損した遺伝子改変マウスでは、アドレナリン受容体阻害薬による神経保護効果は得られなかった。また、アドレナリン受容体阻害薬投与後に脳梗塞を起こし、1時間後に薬を用いてアクアポリン4の機能を一時的に阻害しても、アドレナリン受容体阻害薬の効果は得られなかった。これらの結果は、アドレナリン受容体の阻害による神経保護効果に、アクアポリン4の機能が重要な役割を果たしていることを示している。
イオン選択性微小電極を用いて、大脳皮質細胞外のK+濃度を直接測定した結果、脳梗塞直後から3時間後にわたって通常の4~5倍高い水準のK+が検出された。一方、アドレナリン受容体阻害薬を事前投与した場合は、約60分後に正常な水準に戻っていた。また、アクアポリン4欠損マウスではアドレナリン受容体阻害薬を事前に投与したとしても、K+濃度は高いままだった。
次に、脳梗塞30分後に、トレーサーを脳脊髄液中に注入し、次の30分間でのトレーサーの脳組織内への浸潤を調べた。その結果、脳損傷部位では脳脊髄液の浸潤が通常と比べて小さくなっており、損傷部位では細胞外組織液が滞留していることが示された。一方、アドレナリン受容体阻害薬を事前投与した場合は、正常に浸潤した。
これらのことから、研究グループは、アドレナリン受容体の阻害によってアクアポリン4の局在が確保され、脳脊髄液の移動によって、K+濃度を正常化し、神経保護と脳機能回復を促進するという排出(クリアランス)のモデルを提案。「将来的に、細胞外K+濃度の正常化を標的とした脳梗塞の早期対処法を開発するための橋渡しとなることが期待できる」と、述べている。
▼関連リンク
・理化学研究所 プレスリリース



