網膜色素変性
網膜色素変性は、難病研究疾患に指定されており、光を感知する網膜の中の色素上皮に異常な色素が沈着、光の明るさを感じとる杆体細胞が障害を受ける病気である。詳しい原因は不明で、夜盲、視野の狭窄とともに視力低下が進行してゆく。明るい所から急に暗い所に入ると、その暗さに対応できず、物の見分けがつきにくくなる。遺伝性で、日本では人口10万人に対し18.7人の患者がいると推定されている。進行すると失明にいたるが、進行度合いや症状の現れ方など、個人差があり、すべての患者が失明するわけではない。現時点では適切な治療薬や治療法が確立されていない。
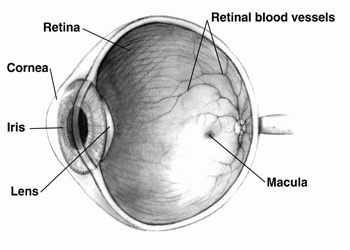
(画像はウィキメディアより)
資金提供をうけ第3相試験へ
アールテック・ウエノは、網膜色素変性治療薬のウノプロストン点眼液に日本の独立行政法人科学技術振興機構からの資金援助をうけ、2013年から国内で第3相試験を実施すると発表した。
ウノプロストンは機能性脂肪酸の一群で、1994年に販売承認を得たレスキュラ®点眼液0.12%(一般名:イソプロピル ウノプロストン)は、緑内障・高眼圧症の治療薬として世界初の「プロストン」医薬品で、発売以来、世界45カ国で承認されている。網膜色素変性に対してもウノプロストンを主成分とした点眼薬の開発中で、第2相試験において、良好な結果が得られている。難病の治療薬として有望視されている薬剤である。(堤朝子)
▼外部リンク
アールテック・ウエノ ニュースリリース2013年3月5日
http://www.rtechueno.com/news/



