げっ歯類でなく「カニクイザル」で神経障害性疼痛モデル樹立、評価方法など検討
北海道大学は5月7日、カニクイザル神経障害性疼痛モデルの評価法構築に成功したと発表した。この研究は、同大大学院歯学研究院の飯村忠浩教授らと、旭化成ファーマ株式会社の共同研究グループによるもの。研究成果は、「Scientific Reports」に掲載されている。
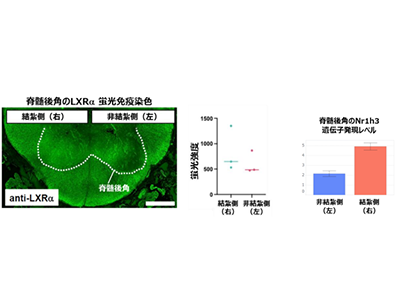
画像はリリースより
(詳細は▼関連リンクからご確認ください)
神経障害性疼痛は、痛みを伝える神経の障害によって引き起こされる痛みで、神経が過敏になり、触っただけで痛みが生じたり、ピリピリ感といった通常とは異なる感覚を生じたりすることもある。しばしば痛みの原因がなくなった後も長期間痛みが続くため、患者の生活の質(QOL)に深刻な影響を与える。これまで神経障害性疼痛の新規治療薬の研究開発は盛んに行われてきた。しかし、動物モデルでは効果があっても実際の患者には効かない事例が多く、新薬開発が難しい疾患とされてきた。その一因として、従来の動物モデルでは、痛みの評価法や疼痛の発生する仕組みに実際の患者との違いがあることで、薬の作用も異なっていた可能性が考えられる。
そこで、今回の研究では、従来、神経障害性疼痛モデルとして広く用いられてきたマウスやラットなどの「げっ歯類」とは異なり、ヒトと同じ「霊長類」のカニクイザルを用いた、神経障害性疼痛の疼痛評価方法や、どの分子が病態に関与しているかについて詳細に検討した。痛みは最終的に脳で感じる。脊髄は背骨の中にある神経の集まりで、脳に痛みの感覚を伝える神経が走る中継地点となっている。感覚を司る神経は、その脊髄から身体のあちこちに張り巡らされている。メスのカニクイザルの片側の脊髄から出る神経を結紮する処置を行うことにより、神経を障害し、神経障害性疼痛の状態を誘発した(サル神経障害性疼痛モデル)。
術後3か月にわたって痛みに関する行動学的解析、脳波解析を実施。また、実際に神経障害性疼痛に使われている薬を投与し、その効果を確認した。さらに、脊髄神経の組織を採取して、遺伝子発現がどのように変化をしているのかを解析し、組織を顕微鏡で観察して実際にどのような分子の発現が変化しているのかを確認した。
疼痛症状と脳波が関連、コレステロールの輸送・代謝の変化が関与の可能性
その結果、サル神経障害性疼痛モデルでは、脊髄神経を障害した側の足にかかる体重が減少し、自発痛を生じていることが観察された。また、その症状の強さは脳波のθ波成分のパワーと相関していた。神経障害性疼痛の患者の脳波においても、θ波成分のパワーが増強していることがすでに報告されている。
さらに、同モデルの脊髄での遺伝子発現を網羅的に調べたところ、炎症関連分子など神経障害性疼痛の発症に重要な分子が増加していることがわかった。これらの分子の中には、これまで小型実験動物(マウスやラット)では変化が観察されることのなかったものが含まれ、一方で、実際の患者で変化している分子も含まれていた。従って、同モデルは実際の患者とより類似した分子メカニズムで神経障害性疼痛を発症していることが考えられた。また、これまでの神経障害性疼痛研究では報告されてこなかったコレステロールの輸送や代謝に関連する分子の変化も新たに発見され、同疾患の新規発症メカニズム解明につながる可能性が考えられた。
今回の研究では、カニクイザル脊髄神経結紮(SNL:Spinal nerve ligation)モデルが神経障害性疼痛の患者と同じように痛みを感じている行動を示すこと、患者と共通した方法で痛みを評価できる可能性があること、その発症の仕組みが患者と共通している可能性が明らかになった。また、神経障害性疼痛の発症にコレステロールの輸送・代謝に携わる分子が介した新しい発症メカニズムの可能性を示した。
神経障害性疼痛への新たな治療薬開発に期待
今回の研究では、カニクイザルを用いた神経障害性疼痛モデルとその評価法を確立した。従来からよく研究に使われた小型動物よりも、より実際の患者に近い神経障害性疼痛モデルとその評価方法によって、神経障害性疼痛の新たな発症メカニズムを発見した。同研究の発展により、神経障害性疼痛に対する新たな治療薬開発につながることが期待される、と研究グループは述べている。
▼関連リンク
・北海道大学 プレスリリース



