A-FMTという新戦略を開発、FMTの効果を最大化する条件を大規模に検証
順天堂大学は4月30日、潰瘍性大腸炎(Ulcerative Colitis:UC)の新たな治療法として注目されている「腸内細菌叢移植療法(Fecal Microbiota Transplantation:FMT)」について、治療効果およびその効果に関与する「良いドナー」の条件、ならびに患者とドナーの腸内細菌叢のマッチングの重要性を明らかにしたと発表した。この研究は、同大大学院医学研究科腸内細菌療法リサーチセンターの石川大センター長、医学部消化器内科学講座の永原章仁教授と、メタジェンセラピューティクス株式会社の山田拓司最高科学顧問らによる研究グループによるもの。研究成果は、「Journal of Crohn’s and Colitis」に掲載されている。また、国際学会(アメリカ消化器病学会、ヨーロッパ腸炎学会、日本消化器病学会など)で口演発表されている。
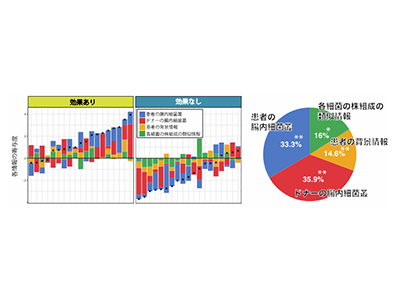
画像はリリースより
(詳細は▼関連リンクからご確認ください)
UCは、腹痛、頻回な下痢、血便を主な症状とする難病指定疾患であり、日本国内には20万人を超える患者がいる。原因はいまだ明らかではなく、過剰な自己免疫反応が関与していることから、現在の治療法は免疫抑制剤やサイトカインを標的とした薬剤療法が中心であり、根本的な治療法は確立されていない。同疾患は腸の粘膜に慢性的な炎症を引き起こし、腸内の有益な細菌が著しく減少することで腸内環境のバランスが崩れることが知られている。
近年、この腸内環境を根本から立て直す新たな治療法として注目されているのがFMTだ。FMTは健康なドナーから提供された便を患者に移植し、多様な腸内細菌を補うことで腸内フローラを再構築する治療法である。しかし、FMTの治療効果には個人差が大きく、「どのドナーが最も適しているのか」「患者とドナーの相性は何によって決まるのか」「治療の最適なタイミングはいつか」など、多くの疑問が未解明のままだった。
このような課題に対して研究グループは、FMTの前処置として抗菌薬を用いることで、患者の腸内に存在する既存の細菌を一時的に除去し、ドナー由来の有用菌がより効果的に定着する環境を整える「抗菌薬併用腸内細菌移植療法(A-FMT)」という新たな戦略を開発した。さらに同研究では、患者ごとに異なるドナーを組み合わせる「1対1戦略」に基づき、FMTの効果を最大化する条件を大規模に検証する研究を行った。
FMT臨床研究に参加した活動期UCの患者97人の治療効果を評価
研究では、便移植前にアモキシシリン、ホスホマイシン、メトロニダゾールの3種類の抗菌薬を2週間服用し、腸内の既存細菌を一時的に減らした上でFMTを行うA-FMTを用いた。この前処置により、ドナー由来の細菌がより定着しやすくなる「腸内の空白地帯(ニッチ)」を形成し、移植効果の増強を目指した。
まず、2014~2019年までにFMT臨床研究に参加した活動期UCの患者97人について、FMT後4週間の症状改善や、12か月以内の再燃の有無などに基づき、短期・長期の治療効果を評価した。さらに、それぞれドナーの異なる患者とドナーの49の組み合わせ、147検体の便サンプル(患者治療前、治療後、ドナー)について、腸内細菌の網羅的な遺伝子解析(16S rRNA遺伝子解析)を実施した。その結果、61人(63%)が臨床的な改善を示し、うち35人(36%)は寛解に至った。興味深いことに、FMTの効果はUCの重症度や過去の薬剤使用歴(ステロイド、免疫抑制剤、生物学的製剤)にも影響されることがわかった。
酪酸産生菌やBacteoridota門の株組成類似性が高いと、FMT後の定着と治療効果「高」
また、有効なドナーにはUC患者で減少している「Bacteroidota門」などの細菌群が豊富に存在していること、反対に、患者自身の腸内由来の細菌や治療後に新たに出現する未同定菌の量が少ないことが、治療成功の指標となることも判明した。
特に「Alistipes」や「Oscillospiraceae UCG-002」などのドナー由来菌が治療効果に強く関連しており、腸内の酪酸産生菌(短鎖脂肪酸を作り出す善玉菌)の存在も効果を左右していることが明らかになった。さらに、患者とドナーの腸内細菌において、特定の酪酸産生菌やBacteoridota門の株組成の類似性が高いほど、FMT後の定着と治療効果が高い傾向にあることも明らかになった。
どの患者に・いつ・どのドナーの便を使用するかという戦略的な判断が、治療成績に影響
今回の研究は、FMTをより効果的に実施するための「最適なドナーの条件」および「患者とのマッチング戦略」を明らかにし、UCに対する個別化医療(プレシジョン・メディスン)としてのFMTの可能性を大きく広げる成果となった。特に、抗菌薬併用FMT(A-FMT)においては、ドナー由来の有用菌が患者の腸内に定着することによって治療効果が得られることが示唆されたが、その定着を成功させるためには、患者側の腸内環境や背景因子との適合性が重要な要素となる。また、Bacteroidota門や酪酸産生菌など、共通した腸内細菌プロファイルを有するドナーがより効果的であることが明らかになった。これにより、今後のドナー選定においては「有効な菌の保有」に加え、「患者との微生物学的な類似性」も重視されることが示唆される。
これらの知見は、FMTを単に実施するだけでなく、「どの患者に・いつ・どのドナーの便を使用するか」といった戦略的な判断が、治療成績に大きく影響することを示している。将来的には、より高精度な腸内細菌叢解析技術と、ドナー・レシピエント間のマッチングアルゴリズムの進展により、個別化FMT治療の標準化と最適化が期待される。本研究結果は、マイクロバイオーム治療の未来に向けて、より精密かつ戦略的な医療アプローチの確立に貢献するものであり、UC患者に対する新たな治療選択肢を提供する重要な一歩となると考えられる。
腸内環境の再構築による新たな治療戦略が、医療の選択肢として確立されることを目指す
腸内細菌サイエンスの飛躍的な進展により、さまざまな疾患の発症や増悪が腸内環境と密接に関係していることが明らかになりつつある。そのような背景のもと、腸内細菌叢を根本的に入れ替えるFMTは、多くの疾患に対して研究・臨床応用が急速に進んでいる。
「今回の研究成果を礎に、より多くの患者に安全かつ効果的な腸内細菌療法を届けられるよう、引き続き精力的に研究と社会実装の両面を推進していく。腸内環境の再構築による新たな治療戦略が、未来の医療の選択肢として確立されることを目指している」と、研究グループは述べている。
▼関連リンク
・順天堂大学 ニュース&イベント



