組換え酵素の大量生産が必要な酵素補充療法、低コストで安全な生産系が課題
京都大学は4月30日、遺伝子組換えカイコで産生したヒトライソゾーム酵素のN型糖鎖をエンドグリコシダーゼにより改変し、ムコ多糖症I型(MPS I)ニホンザルの臨床徴候を改善することに成功したと発表した。この研究は、同大ヒト行動進化研究センターの大石高生准教授、徳島大学大学院薬学研究科の篠田知果博士前期課程学生(当時)、伊藤孝司名誉教授、川崎医科大学の北風圭介助教、国立研究開発法人農業・食品産業技術総合研究機構、国立医薬品食品衛生研究所、株式会社伏見製薬所、金沢大学、兵庫県立大学、自然科学研究機構、岐阜大学、神戸薬科大学の研究グループによるもの。研究成果は、「Communications Medicine」にオンライン掲載されている。
画像はリリースより
(詳細は▼関連リンクからご確認ください)
ライソゾーム病はライソゾーム酵素の遺伝的欠損を原因とする疾患群で、ムコ多糖症はムコ多糖を分解するライソゾーム酵素が生まれつき欠損することで全身の細胞にムコ多糖が蓄積する疾患だ。MPS Iは、ライソゾーム酵素であるα-L-イズロニダーゼ(IDUA)遺伝子の変異によって引き起こされ、IDUAによって分解されるグリコサミノグリカン(GAG)のデルマタン硫酸やヘパラン硫酸が細胞内外に過剰に蓄積し、全身性の臨床症状を引き起こす。MPS Iに対する治療法の一つは、哺乳類細胞株で産生した組換えヒトIDUA(一般名:ラロニダーゼ)を静脈内投与する酵素補充療法だ。しかしながら、組換えライソゾーム酵素を大量に生産する必要があるため、より低コストかつ安全な生産系が求められている。
組換えカイコ発現系でヒトIDUAを大量精製し糖鎖改変、ニホンザルモデルで治療効果確認
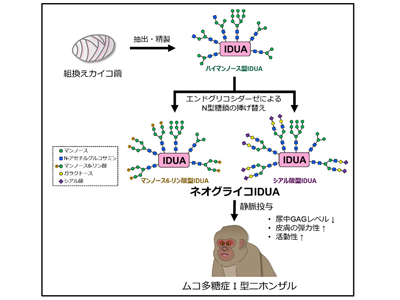
研究グループは遺伝子組換えカイコ発現系を用い、カイコ繭から組換えヒトIDUAを大量に抽出・精製することに成功した。精製IDUAにはライソゾーム酵素の細胞内取り込みに必要なマンノース6-リン酸(M6P)含有N型糖鎖は含まれていなかったことから、エンドグリコシダーゼを用いてN型糖鎖を改変したM6P型IDUA(M6P-IDUA)を調製した。また、近年ムコ多糖症VII型の治療用酵素であるベストロニダーゼ・アルファでは、酵素に付加されたシアル酸含有N型糖鎖が細胞内取り込みや薬物動態を改善することが示唆されていることから、シアル酸型IDUA(SG-IDUA)も調製した。
一方、京都大学ヒト行動進化研究センターで集団継代飼育されているニホンザル群の中から、軽症/中間型MPS Iの臨床徴候を示す個体を発見し、IDUA遺伝子のミスセンス変異(一塩基変異)を同定した。さらに、MPS IニホンザルにM6P-IDUAあるいはSG-IDUAを静脈内投与することで、尿中GAGを減少させ、臨床徴候を改善させることに成功した。以上から、遺伝子組換えカイコとエンドグリコシダーゼの組み合わせは、機能的なN型糖鎖を有するデザイナー糖タンパク質(ネオグライコ酵素)を生産するための有望なアプローチであると考えられる。
MPS Iニホンザル、遺伝子治療開発にも応用できる可能性
エンドグリコシダーゼ処理はコストパフォーマンス面の改善が必要だ。今後、遺伝子組換えカイコに哺乳類型糖転移酵素遺伝子群を導入することでN型糖鎖構造をヒト型化し、低コストでのヒト糖タンパク質製造プラットフォームを構築したいと考えている。「また、MPS Iニホンザルはヒトと共通した原因・症状・治療法の条件を満たす疾患モデルと考えられることから、遺伝子治療法などの開発研究にも応用したいと考えている」と、研究グループは述べている。
▼関連リンク
・京都大学 最新の研究成果を知る



