治療の選択肢が広がるAD、患者ごとの背景に基づくエンドタイプ分類方法は未確立
理化学研究所(理研)は10月20日、アトピー性皮膚炎(AD:atopic dermatitis)患者の複数の形質に関わる病態の違いを同定したと発表した。この研究は、理研生命医科学研究センター免疫器官形成研究チームの関田愛子研究員、川崎洋上級研究員、古関明彦チームリーダー、皮膚恒常性研究チームの天谷雅行チームリーダー(慶應義塾大学医学部皮膚科学教室教授)、システム遺伝学チームの岡田随象チームリーダー(大阪大学大学院医学系研究科遺伝統計学教授)らの研究グループによるもの。研究成果は、「Nature Communications」にオンライン掲載されている。
画像はリリースより
(詳細は▼関連リンクからご確認ください)
ADは、皮膚機能や免疫システムの異常により誘発される慢性の炎症性皮膚疾患である。患者によって異なる遺伝的・後天的要素が絡み合ってさまざまな臨床症状を引き起こす。ADは、症状の違いによる分類の他に、症状の原因となる遺伝的特徴や生理学的背景などに基づく分類が可能であると考えられている。このような分類をエンドタイプと呼び、特定の治療に対する患者ごとの効果の違いに強く関連すると考えられている。しかし、エンドタイプの分類方法は確立されておらず、どの患者にも一様に、皮膚の炎症を抑えるステロイドなどの抗炎症治療薬が主に使われてきた。近年、新たな分子標的薬が次々に開発され、治療の選択肢が広がっているが、それぞれの患者に合った治療を選択するための知見は十分に得られていない。このため、患者から計測される指標(バイオマーカー)によって各患者の病態の特性を規定した上で、最適化した治療・予防法を提案する個別化医療の実現が求められている。
また、大部分の患者は長年にわたり寛解と増悪を繰り返す。ある一時点の症状の評価だけでは患者の特徴を十分に捉えきれていない可能性がある。このため同一患者の症状の経時的変動を理解した上で予測医療につなげることが期待されている。
全身的な免疫システムや細かいレベルでの症状を考慮した病態多様性の理解が必要
このようなADの病態の多様性を理解するには、患者に起きている皮膚の機能的変化および全身の免疫状態を調べる必要がある。組織の遺伝子発現情報は、このような個人の生物学的変化を詳細に評価する有用な指標である。しかし、過去の遺伝子解析研究では、1人の患者からの血液または皮膚組織のみのデータでしか解析されていなかったため、ADにおける全身的な免疫システムの多様性を十分に解明できていなかった。症状と分子病態の関連についても、皮膚炎の症状が重症か軽症かという単純な評価が使われるだけで、どのような性状の皮疹を来すかといった、より細かいレベルでの症状の多様性が考慮されることはなかった。
AD患者では皮膚-血液の相互作用が増大と判明、両者の遺伝子発現の統合解析が重要
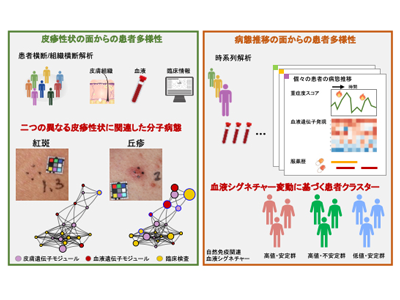
そこで今回の研究では、紅斑と丘疹という2種類の特徴的な皮疹性状に着目し、これらと特定の遺伝子発現の関係性からADの病態多様性を解明することを目指した。また、症状の経時的変化と遺伝子発現変動パターンの関連の解明を試みた。研究グループはまず、AD患者115人と健常者14人の被験者の皮膚組織および血液のRNAシーケンスを行い、各組織における遺伝子発現量を網羅的に調べた。
AD患者における皮膚組織と血液の組織間の相互作用を調べるために、サイトカインなどの可溶性因子とその受容体の遺伝子が同時に発現している状態(共発現)に着目した組織間相互作用解析を行った。その結果、AD患者群では健常群に比べて、皮膚-皮膚の組織内相互作用に加えて皮膚-血液の組織間相互作用の度合いが増大していることが示された。すなわち、ADの病態には皮膚組織と血液が互いに作用しながら関与しており、両者の遺伝子発現量を統合して解析することが病態解明に重要と考えられた。
共発現する遺伝子群を定義したモジュール、AD患者皮膚組織で21血液では15を同定
異なる組織のRNAシーケンスデータは、発現量の分布が大きく違うため、皮膚と血液の絶対発現量を単純に結合すると解釈が難しくなる。また、RNAシーケンスでは2万個程度の遺伝子の発現データが得られるため、複数組織のデータを合わせると、発現量の関係を解析する指標の数(次元数)が膨大になってしまう。
そこで研究グループは、各組織における遺伝子発現量を、遺伝子間の共発現の大きさに基づき次元圧縮した。AD患者横断データを用いて、共発現する遺伝子同士を一つのグループにまとめる遺伝子発現モジュールを定義することにより、データ次元数を大幅に削減できるだけでなく、ADに特徴的な遺伝子発現パターンを強調することができる。この解析では、皮膚組織で21モジュール、血液で15モジュールをそれぞれ同定できた。これらのモジュールを構成する遺伝子群は、各免疫細胞種や皮膚細胞種に特異的な発現パターンを持つこと、また免疫制御や代謝など特定の分子の反応に関わっていることが、公共データベース上のデータを活用した解析により明らかになった。すなわち、これらのモジュールはADの病態に関連する生物学的機能を反映した遺伝子の集団であると示唆された。
紅斑と丘疹ではそれぞれ異なる遺伝子発現パターンが寄与
次に、研究グループは、病型多様性の一つの切り口として、2種類の皮疹性状(紅斑、丘疹)に着目し、それぞれの皮疹性状の度合いと皮膚組織の遺伝子発現モジュールの関係性を解析した。
その結果、紅斑には、皮膚のケラチノサイト、皮膚に分布する単球や樹状細胞、および血液の制御性T細胞で主に発現するモジュールが寄与していることが明らかになった。一方、丘疹には、血液のB細胞、血液のCD4陽性T細胞、皮膚の血管内皮細胞、および皮膚の線維芽細胞で主に発現するモジュールが寄与していた。これらのことから、ADとしてひとくくりにされてきた多様な皮疹性状の根底には異なる分子病態が存在することが示された。
30人の1年間にわたる血液時系列データから、寛解や増悪に関わる3つのクラスターに分類
また、30人のAD患者について、1年間にわたる血液時系列データを解析し、病勢パターンと遺伝子発現変動パターンの関連解析を行った。まず、血液遺伝子発現の時系列特徴量で患者を分類したところ、自然免疫に関わる分子シグナチャーが1年間にわたり(1)比較的高値で安定なクラスター、(2)高値と低値の変動が大きいクラスター、(3)比較的低値で安定なクラスターに分かれた。これらの患者の症状の時系列特徴量を照らし合わせると、症状の推移は、クラスター(1)では比較的重症な状態が継続的に続く、クラスター(2)では寛解と増悪を繰り返す、クラスター(3)では比較的軽症な状態を維持していることがわかった。さらに、クラスター(1)の患者は免疫抑制剤の服用歴のある患者が多く、いわゆる難治性ADと高度に重複していることが示唆された。以上のことから、患者ごとの寛解と増悪といった病勢のパターンと遺伝子発現変動パターンが関連することと、これが患者の治療履歴を反映していることが示された。
広範囲の臨床情報や生体分子の網羅的情報を統合解析し、個別化医療の実践へ
ADについては、今回着目した皮疹性状や病態推移の観点以外にも、気管支喘息などの合併症の有無や遺伝的素因といったさまざまな切り口からの患者病態の多様性を議論できると考えられる。「今後は、より広範囲の臨床情報および生体分子の網羅的情報を統合し解析することで、患者の多様性およびADのエンドタイプについて理解を深めるとともに、各患者の治療標的の同定を通して個別化医療の実践につなげることが期待される」と、研究グループは述べている。
▼関連リンク
・理化学研究所 プレスリリース



