後縦靭帯が骨に変化し運動障害を引き起こすOPLL、発症頻度は高いが根本的な治療法はない
理化学研究所(理研)は4月3日、後縦靭帯骨化症(OPLL)の発症に関わる遺伝子「CCDC91」を発見し、分子レベルでその作用を明らかにしたと発表した。この研究は、理研生命医科学研究センター骨関節疾患研究チームの池川志郎チームリーダー(研究当時)、ゲノム解析応用研究チームの寺尾知可史チームリーダー、小井土大客員研究員らの研究グループによるもの。研究成果は、「American Journal of Human Genetics」にオンライン掲載されている。
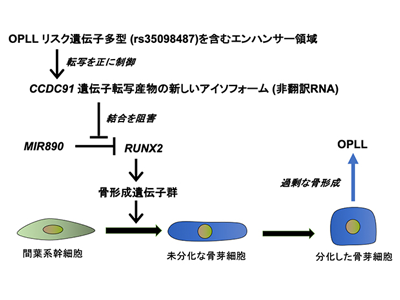
画像はリリースより
(詳細は▼関連リンクからご確認ください)
骨、関節をはじめとする運動器の疾患には、多くの遺伝性難病が含まれている。研究グループは、運動器の遺伝性難病の原因遺伝子の同定を出発点として、原因遺伝子とその変異の機能解析を通じて画期的な診断法・治療法を開発するとともに、骨格や運動器の成長・発達・維持のメカニズムの解明を目指し、研究を続けてきた。これまでに、数多くの運動器疾患の原因遺伝子を発見し、その分子病態を明らかにしてきた。
OPLLは、背骨の椎体の後面を縦に走る後縦靭帯が骨に変化し、そのすぐ後ろにある脊髄や神経を圧迫して、手や足のしびれや痛み、運動障害などさまざまな症状を引き起こす疾患である。50歳前後で発症することが多い、極めて頻度の高い疾患で、日本での患者数は100万人以上と考えられている。しかし、現在のところ根本的な治療法はなく、厚生労働省が定める指定難病となっている。
OPLLのGWAS結果から発見されたリスク遺伝子多型が発現に影響するRNAを探索
過去の疫学研究から、OPLLの発症・進行には遺伝的要因が関与すると考えられ、日本を中心に原因遺伝子の探索が行われてきた。2014年、研究グループは日本の患者を対象としたOPLLのゲノムワイド関連解析(GWAS)を行い、発症しやすさ(疾患感受性)に関わるゲノム領域を複数発見した。今回の研究では、OPLLの疾患感受性遺伝子とその多型(個人差)の同定を行った。
研究グループは2022年、DNA配列の変化による非翻訳RNA発現量の変化を機械学習によって予測するMENTR(Mutation Effect prediction on NcRNA TRanscription)法を開発していた。このMENTR法を2014年のOPLLのGWAS結果に適用したところ、軟骨細胞、骨芽細胞、間葉系幹細胞などのOPLL関連細胞において、6個のCAGEタグ(mRNAの5’末端の約20塩基の配列)の発現が計12個のOPLLの疾患感受性(リスク)遺伝子多型と相関することがわかった。それらのリスク遺伝子多型のうちrs35098487は「CCDC91(coiled coil domain 91)遺伝子」領域内に存在し、他のCAGEタグ「p4@CCDC91」の発現に影響していた。
発見されたアイソフォームは各組織で強く発現する「ノンストップmRNA」
CCDC91遺伝子には、22個の転写産物アイソフォームが存在することが知られている。しかし、p4@CCDC91の配列はそれら既知のアイソフォームのどれとも一致せず、「新しいアイソフォーム」の転写開始点の塩基配列であることがわかった。そこで、リアルタイムPCR法と3′-RACEというin vitro(試験管内で)の実験手法を用いて、この新しいアイソフォームの全長を同定した。このアイソフォームは、大多数の既知のアイソフォームと同じ翻訳開始点を持っているが、翻訳の読み枠には終止コドンがなく、翻訳領域の途中にポリA(アデノシンが複数連続した配列)が付加された「ノンストップmRNA」だった。一般に、ノンストップmRNAはノンストップmRNA decayという機構により転写後すぐに分解され、消失するとされている。しかし、この新しいアイソフォームは脳、腎臓、腱、靭帯などの組織で強く発現していた。
5′-UTRのリスクアレルが転写活性に影響、アイソフォーム発現は骨芽細胞の分化初期に亢進
rs35098487は新しいアイソフォームの5′-UTR(5’非翻訳領域)部分に存在した。5′-UTRは遺伝子の転写に関わることが多いため、この遺伝子多型の転写への影響を実験で調べた。すると、rs35098487のOPLLリスクアレルは、非リスクアレルに比べてより強く核内タンパク質と結合し、強い転写活性を示した。
骨芽細胞は骨形成の主役となる細胞で、間葉系幹細胞から分化する。新しいアイソフォームの発現をOPLLに関係するさまざまな組織・細胞で実験的に調べたところ、骨芽細胞分化で中心的な役割を果たすRUNX2遺伝子と並行して、新しいアイソフォームの発現が骨芽細胞の分化の初期に亢進することがわかった。間葉系幹細胞やMG-63などの骨形成株化細胞で、新しいアイソフォームの発現をsiRNAで阻害すると、RUNX2遺伝子をはじめとする骨形成関連遺伝子群の発現が低下した。一方、新しいアイソフォームを過剰に発現させると、骨形成関連遺伝子群の発現、ならびに骨形成が上昇した。
RUNX2遺伝子の機能を抑制するマイクロRNAと新アイソフォームが結合、骨形成を亢進させる
次に、RNA22 V2(ゲノム上のマイクロRNAの結合部位を予測)とmiRDB(マイクロRNAのターゲット予測と機能アノテーション)によるin silico解析から、新しいアイソフォームはマイクロRNA(miRNA)との結合部位を持ち、MIR890というmiRNAと結合することが予測され、ルシフェラーゼアッセイでそれが証明された。MIR890はRUNX2遺伝子の3′-UTR(3’非翻訳領域)と結合し、RUNX2遺伝子の機能を抑制した。
以上の結果から、CCDC91遺伝子によるOPLLの発症のしやすさのメカニズムは次のように考えられる。1)CCDC91遺伝子転写産物の新しいアイソフォームは、非翻訳RNAとしてMIR890と直接結合し、MIR890とRUNX2遺伝子の結合を阻害することで、骨芽細胞の分化の初期過程において骨形成を亢進させる。2)リスク遺伝子多型のrs35098487は、新しいアイソフォームの発現を上昇させる。
同様の研究手法の融合アプローチ、さまざまな疾患感受性遺伝子の発見につながると期待
これまでさまざまな疾患でGWASが行われてきたが、実際に疾患感受性遺伝子の同定に成功する例はごく少数だった。しかし今回、AIを活用した統計学的解析による予測と骨代謝学・分子遺伝学に関する専門的な実験による検証により、それが可能になった。今後、同様のin silicoとin vitroの研究手法の融合アプローチにより、さまざまな疾患感受性遺伝子が発見されると期待できる。
今回の結果は、靭帯細胞に特異的に発現する非翻訳RNAのネットワークが、骨形成の制御を通じて、OPLLの発症・進展に重要な役割を担うことを示している。「今後、CCDC91-MIR890経路の骨形成における役割を詳しく調べることで、OPLLの病態の理解が進み、新しいタイプの治療薬が開発されると期待できる」と、研究グループは述べている。
▼関連リンク
・理化学研究所 プレスリリース



