「内軟骨性骨化」と「膜性骨化」は独立した現象と考えられてきた
東京大学は7月20日、骨を太くする「骨膜幹細胞」が、骨を長くする「成長板幹細胞」を遠隔からコントロールすることで、生後の骨格成長に重要な役割を果たすことを世界で初めて発見したと発表した。この研究は、同大大学院医学系研究科 病因・病理学専攻 免疫学分野の塚崎雅之特任助教と高柳広教授らの研究グループによるもの。研究成果は「Nature Communications」に掲載されている。
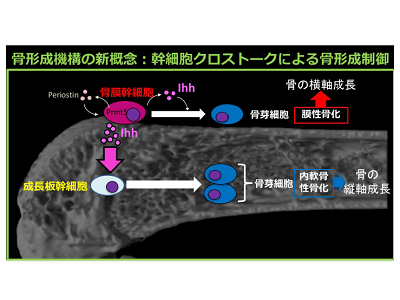
画像はリリースより
(詳細は▼関連リンクからご確認ください)
脊椎動物の「かたち」を決定している骨格系は、身体を支え運動を可能とする運動器としての役割だけでなく、ミネラル代謝調節や造血といった多様な機能を併せ持ち、生体恒常性の維持に必須の役割を担っている。四肢を構成する長管骨の縦軸方向への成長は、骨内部の成長板軟骨に存在する成長板幹細胞が増殖・分化を繰り返すことにより駆動されており、このプロセスは「内軟骨性骨化」と呼ばれ、個体のサイズを決定づける。一方、頭蓋骨および鎖骨の形成と、長管骨の横軸方向への成長は、骨の外周を包む骨膜に存在する骨膜幹細胞により仲介され、このプロセスは軟骨形成を伴わないことから「膜性骨化」と呼ばれている。
生後の急激な身長の増加は、乳幼児期、学童期、思春期にそれぞれ栄養、成長ホルモン、性ホルモンが直接的・間接的に成長板軟骨に作用することにより実現され、思春期以降の骨端線の閉鎖(成長板軟骨の癒合)により停止すると考えられている。しかし、内軟骨性骨化による適切な骨成長の維持機構および骨端線閉鎖の分子機構に関して不明な点が多く、さまざまな原因で生じる低身長症に対する有効な予防・治療法の開発が重要な課題となっている。また、内軟骨性骨化と膜性骨化は、それぞれ局在の異なる骨格幹細胞によって制御される独立した現象と考えられており、骨膜幹細胞と成長板幹細胞の関係性や相互作用に関してはこれまでわかっていなかった。
骨格幹細胞の運命についての研究は進んでいるが、他の細胞との相互作用の可能性は?
近年、成長板幹細胞と骨膜幹細胞がマウス骨組織より単離・解析され、局在と性質の異なる骨格幹細胞が、それぞれ局所的に増殖・分化することで、内軟骨性骨化と膜性骨化を制御するという概念が提唱された。世界中で、骨格幹細胞の運命(どこからやってきて、どこで、どのような細胞に分化してゆくか)に関する研究が精力的に行われている一方で、骨格幹細胞が可溶性因子を分泌し、他の細胞と相互作用する可能性に関しては調べられていない。
成長板幹細胞が適切に維持されるためには、骨化制御因子Indian Hedgehog(Ihh)のシグナルを受け取る必要があり、成長板幹細胞の子孫細胞である肥大軟骨細胞がIhhを発現していることが知られていた。しかし、他の細胞が産生するIhhが成長板幹細胞を制御する可能性に関しては検証されていなかった。
骨膜幹細胞の数が減ると膜性骨化だけでなく内軟骨性骨化も障害、モデルマウスで
研究グループははじめに、タンパク質修飾酵素のひとつであるPRMT5の破骨細胞における機能を探索する目的で、Cathepsin K(CtsK)-Creを用いて、PRMT5遺伝子をカテプシンK発現細胞で特異的に除去したマウス(PRMT5flox/Δ CtsK-Cre)を作製した。カテプシンKは破骨細胞が骨の有機質を分解するために使用するタンパク質分解酵素であり、CtsK-Creは破骨細胞で特異的に遺伝子を除去するシステムと考えられていた。作製したマウスでは、内軟骨性骨化と膜性骨化の両方が障害され骨成長障害を呈したものの、意外なことに破骨細胞の分化や機能、遺伝子発現プロファイルは全く変化しておらず、骨成長障害はCtsK-Creが他の細胞でPRMT5遺伝子を除去したことによる影響と考えられた。
原因を探索した結果、CtsK-Creが骨膜幹細胞でも作動していること、骨膜幹細胞でPRMT5が除去されると、生後徐々に骨膜幹細胞の数が減少してゆくことを突き止めた。研究グループは、期せずして骨膜幹細胞の数が生後減少するマウスを作出し、骨膜幹細胞の数が減ると膜性骨化だけでなく内軟骨性骨化も障害されるという意外な事実を発見した。
骨膜幹細胞は可溶性の骨化制御因子Ihhを高発現
これまで、骨膜幹細胞が膜性骨化にのみ寄与すると考えられてきた理由は、1)骨膜幹細胞の子孫細胞は、骨内部には侵入せず骨外膜に限局する、2)骨膜幹細胞で骨形成に必須の遺伝子Osterixを除去すると、膜性骨化のみが障害される、3)骨膜幹細胞を異所性に移植すると、膜性骨化のみ引き起こす、という3つの根拠によるものだった。しかし、骨膜幹細胞が可溶性因子を分泌することで遠隔的に内軟骨性骨化を制御する可能性に関しては見落とされていた。そこで、骨膜幹細胞で高発現する可溶性因子を探索し、骨化制御因子Ihhを同定した。
可溶性因子を介した幹細胞クロストークが生後の骨成長を制御
胎生期の骨組織を用いた組織学的解析により、成長板軟骨の一部である肥大軟骨細胞がIhhを高発現することが報告されており、主要なIhh産生源と考えられてきた。他の細胞が発現するIhhの役割については不明であったため、骨膜幹細胞でIhhを除去したマウスを作製したところ、成長版幹細胞の増殖が阻害され、3週齢(ヒトだと幼児期)以降に重篤な骨成長障害を呈することがわかった。
肥大軟骨細胞でIhhを除去したマウスも作製し解析したところ、3週齢より以前に重篤な骨形成障害を起こすことが明らかとなり、胎生〜幼児期といった早期ライフステージにおいては、肥大軟骨細胞由来のIhhが重要であるものの、生後に肥大軟骨細胞が退縮するに伴い、骨膜幹細胞由来のIhhが適切な骨成長に寄与する可能性が考えられた。
以上から、可溶性因子を介した幹細胞クロストークが生後の骨成長を制御するという新たな概念が創出され、膜性骨化と内軟骨性骨化システムは互いに相互作用しつつ複雑な骨格系を形成している可能性が示唆された。
骨膜を標的とした新しい骨再生療法の開発や、低身長症などの治療法確立に期待
今回の研究により、異なる幹細胞間の相互作用が、骨の成長に寄与すること明らかとなった。性質や局在の異なる組織幹細胞同士のクロストークの重要性は、ハエの生殖器や哺乳類の皮膚といった組織においても報告されており、「幹細胞クロストーク」は複雑な臓器を形づくり維持してゆくための根源的な機構である可能性が示唆される。進化的には、膜性骨化は内軟骨性骨化よりも古くから存在するシステムと考えられており、膜性骨化を担う幹細胞が別の骨化システムを制御し骨格形成を司るという知見は、脊椎動物の進化を理解する上でも重要な示唆を含む。
「今回の成果は、骨折や骨再生の手術の際に、骨膜を保存することが重要である根拠の一つを解明したものであり、骨膜を標的とした新しい骨再生療法の開発や、低身長症、骨粗鬆症、難治骨折、骨腫瘍などさまざまな骨病態に対する治療法の確立に貢献することが期待される」と、研究グループは述べている。
▼関連リンク
・東京大学大学院医学系研究科 プレスリリース



