TNBC治療、化学療法抵抗性を解除する新たな治療法が望まれている
北海道大学は10月20日、トリプルネガティブ乳がん(TNBC)において、がん細胞が分泌するインターロイキン-34(IL-34)が強い免疫抑制と抗がん剤抵抗性をもたらすことを発見したと発表した。この研究は、同大遺伝子病制御研究所病態研究部門免疫生物分野の清野研一郎教授、梶原ナビール氏らの研究グループと、同大大学院医学院組織細胞学教室、同大病院乳腺外科、大阪ろうさい病院乳腺外科、同大医学部分子生物学教室との共同研究によるもの。研究成果は、「Cancer Immunology, Immunotherapy」に掲載されている。
画像はリリースより
(詳細は▼関連リンクからご確認ください)
乳がんは世界中の女性において、罹患率・死亡率ともに最も高い悪性腫瘍の1つ。また、乳がんは、がん細胞の表面に出ている受容体の種類によって大きく4つのタイプに分けられ、それぞれのタイプによって治療法が大きく変わってくる。タイプ別に分けたときの1つであるTNBCは、乳がんの治療標的となる3つの受容体が欠如していることから、そのように名付けられており、全乳がんの約20%を占める。TNBCは他のタイプの乳がんと比較して、より高い再発率、再発後の急速な進行を示し、予後不良だ。TNBCに対する薬剤治療としては、抗がん剤を用いた化学療法が一般的であるが、多くの患者が化学療法に対する抵抗性を獲得してしまうため、その抵抗性を解除するような治療法・治療薬の開発が強く望まれている。
化学療法抵抗性への寄与が判明しているMDSCに着目
研究グループは、腫瘍中に浸潤する免疫細胞の中で最も多くを占める骨髄由来抑制細胞(MDSC)という免疫細胞に注目した。MDSCは、強い免疫抑制能を持つものや血管新生能を持つものなどさまざまな機能を持つ細胞で構成される雑多な細胞集団であり、腫瘍環境においては、複数の側面で重要な役割を担っている。また、化学療法に対する抵抗性獲得への寄与も明らかになっている。近年は、腫瘍内のMDSCを制御することが新たながんの治療法の1つとして注目を浴びており、世界中で数多くの研究が行われている。
TNBCで高発現のIL-34、詳細な役割と化学療法の効果に及ぼす影響を検討
腫瘍環境の免疫抑制に寄与する因子として、IL-34というタンパク質が報告されている。研究グループはこれまでに、さまざまながん種の腫瘍組織においてIL-34の発現を確認しており、がん細胞から産生されるIL-34が、がんの悪性度に関わることや、がんの進行を促進することを明らかにしてきた。特に、TNBCにおけるIL-34の発現は他のタイプの乳がんよりも高く、IL-34の高発現が単独でTNBC患者の予後不良因子となることを明らかにしている。さらに、実験用マウスを使った実験によりIL34がTNBC腫瘍の成長を促進することもわかっている。一方、TNBCにおいてIL-34がどのように腫瘍の成長を促進し予後不良に影響するのか、そのメカニズムは解明されていなかった。
そこで、今回の研究では、TNBCの腫瘍組織におけるIL-34の詳細な役割と、化学療法の効果に及ぼす影響を検討した。研究の推進により、新規がん治療コンセプトが生まれる可能性があり、社会的意義があると考えられる。
IL-34産生/欠損マウスや患者から採取したTNBC腫瘍組織を用いて解析
まず、IL-34を発現するマウスTNBC細胞株である4T1細胞を用いて、TNBCにおいてIL34が腫瘍成長を促進する機序について調べた。IL-34を欠損させた4T1細胞を樹立し、それとIL-34を発現する細胞をそれぞれ別の実験用マウスの皮下に注入することで、担がんマウスを作製した。その後、マウス生体内で増殖した各腫瘍内に浸潤している免疫細胞の種類や量を解析することで、がん細胞から産生されるIL-34がTNBCの腫瘍環境にどのような影響を与えるのかを検証した。さらに、TNBCを自然発がんするマウスや患者由来乳がん組織から構築したオルガノイドにIL-34の阻害薬を投与し、同様の解析を行った。
次に、IL-34を産生もしくは欠損した細胞を実験用マウスの皮下に注入し、抗がん剤を投与することで、TNBC腫瘍から産生されるIL-34が化学療法の効果に与える影響を調べた。また、1,083人の乳がん患者の臨床情報(腫瘍組織における遺伝子発現情報)をもとに、全乳がん患者を4つのタイプ別(TNBC、HER2+、LuminalA、LuminalB)に分類し、マウス実験にて得られた結果がTNBC患者のリアルな腫瘍環境をどの程度反映しているか検討。加えて、35人のTNBC患者から新たに得られた腫瘍組織を用いて上記の結果の外挿性を評価した。
IL-34がM-MDSCとPMN-MDSCのバランスを直接調節
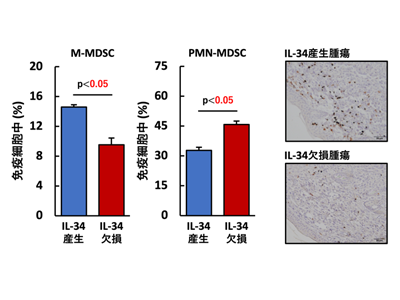
IL-34を発現する4T1細胞でできた腫瘍と、IL-34を欠損させた4T1細胞でできた腫瘍に浸潤している免疫細胞の種類や量を比較したところ、MDSCの浸潤率、中でも単球系MDSC(M-MDSC)と多形核MDSC(PMN-MDSC)の浸潤レベルに大きな差が観察された。具体的には、IL-34産生腫瘍ではIL-34欠損腫瘍と比較してM-MDSCが顕著に増加し、PMN-MDSCが減少していた。
各MDSCの浸潤率の差がIL34による直接的なものかどうかを調べるために、試験管内で骨髄からMDSCを誘導する実験系にIL-34を添加したところ、IL-34が骨髄からM-MDSCの分化を誘導しPMN-MDSCへの分化を抑制することが明らかになった。すなわち、腫瘍環境においてTNBC細胞が産生するIL-34がM-MDSCとPMN-MDSCのバランスを直接調節していると考えられた。
TNBCのIL-34は強力な免疫抑制と抗がん剤抵抗性を誘導
M-MDSCは自身が強力な免疫抑制能を持つだけでなく制御性T細胞などの他の免疫抑制細胞を引き寄せることがわかっているため、IL-34産生もしくは欠損腫瘍における制御性T細胞の浸潤レベルを解析したところ、IL-34欠損腫瘍において制御性T細胞浸潤の劇的な減少が観察された。また近年、PMN-MDSCと血管新生との間に深い関係があることがわかっており、IL-34産生/欠損両腫瘍における腫瘍内血管量を比較したところ、IL-34欠損腫瘍における血管浸潤の大幅な増加が観察された。腫瘍内の血管は無治療時、がん細胞に栄養を運びがんの成長を手助けする一方で、治療時には薬剤の送達性を上げる。よってIL-34を産生もしくは欠損した細胞を実験用マウスの皮下に注入し、それらのマウスに抗がん剤を投与したところ、もともと抗がん剤が全く効果を示さなかったIL-34欠損腫瘍の成長が有意に抑制された。以上の結果は、TNBCの腫瘍環境におけるIL-34-MDSC軸を介した免疫抑制と化学療法抵抗性の存在を示唆している。
IL-34阻害薬で、腫瘍内の免疫抑制と化学療法抵抗性を解除できる可能性
また、TNBCを自然発がんするマウスや患者由来乳がん組織から構築したオルガノイドにIL-34阻害薬を投与し、腫瘍内に浸潤するMDSCを解析したところ、M-MDSCの減少とPMN-MDSCの増加が観察されたことから、IL-34を標的とした治療により腫瘍内の免疫抑制と化学療法抵抗性を解除できる可能性が示された。
まとめると、IL-34がTNBC腫瘍の成長を促進するメカニズムの1つとして、IL-34自身がM-MDSCとPMN-MDSCのバランスを調節し、それにより免疫抑制および化学療法抵抗性を誘導することを明らかにした。
今回の研究によって、TNBCにおいてIL-34がMDSCを介して腫瘍の成長および予後不良をもたらすことが示された。したがって、IL-34を標的とした治療は、TNBC患者の予後を改善する可能性がある。「今後、「TNBC局所におけるIL-34の発現診断→IL-34阻害薬の投与」という新しいがん治療のコンセプトが生まれる可能性がある。IL-34阻害薬の開発が進み、臨床応用されることが期待される」と、研究グループは述べている。
▼関連リンク
・北海道大学 プレスリリース



