中枢神経系の発達過程で「低酸素状態」が髄鞘化の発達を促進、末梢神経では?
国立精神・神経医療研究センター(NCNP)は8月14日、低酸素状態が末梢神経損傷後の再生を促進するメカニズムを解明したと発表した。この研究は、NCNP神経研究所疾病研究第五部の荒木敏之部長・若月修二室長・氏家悠佳研究員、九州大学の大川恭行教授・原田哲仁教授、早稲田大学の合田亘人教授らの研究グループによるもの。研究成果は、「Journal of Biological Chemistry」オンライン版に掲載されている。
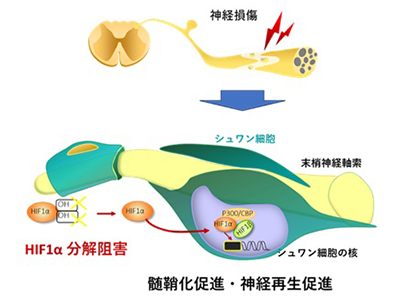
画像はリリースより
(詳細は▼関連リンクからご確認ください)
神経細胞は単独では効率的な情報伝達を行うことができず、長い突起を介した素早いシグナル伝搬のためには、神経突起の周囲が髄鞘(ミエリン)と呼ばれる構造物により取り巻かれることが必要だ。
髄鞘は、中枢神経系(脳・脊髄)では希突起膠細胞(オリゴデンドロサイト)、末梢神経ではシュワン細胞と呼ばれる細胞によって形成され、いずれの場合もそれぞれの細胞の細胞膜が幾重にも重なってぐるぐる巻きついたものが髄鞘だ。細胞膜は脂質によって形成されていることから髄鞘は絶縁体として機能し、神経突起は絶縁体によって取り巻かれることによって「跳躍伝導」と呼ばれる速い電気シグナルの伝達が可能となる。この髄鞘は、主に生後発達の過程において、個体を取り巻く多様な環境の影響を受けながら形成が進み、神経伝導の効率化を通じて、運動制御や感覚機能の発達に寄与すると考えられている。
中枢神経系の発達過程において、「低酸素状態」がオリゴデンドロサイトによる髄鞘化の発達を促進する作用を持っていることが、過去の論文で報告されている。ここでいう「低酸素状態」とは、病気や事故などによって引き起こされるような著しい酸素不足ではなく、通常の酸素環境・定型的な発達の中で起こる組織中の酸素濃度の変動によって起こるものである。一方、末梢神経系では、このような生理的に起こる酸素濃度変動の影響は知られていなかった。
低酸素環境下ではHIF1α「増」で髄鞘が作られやすく、HIF1α「少」で神経回復遅延
研究グループは、主に4つのことを明らかにした。HIF1αは、低酸素状態になると存在量が増え機能できるようになる。同研究グループは、マウスの後根神経節を使って作成した細胞培養に神経軸索の髄鞘化を観察する実験システムを用いて、低酸素環境下もしくはHIF1αの分解を阻害する薬剤を投与した場合にはシュワン細胞でHIF1αが増え、髄鞘化の促進がみられることを示した。これにより、低酸素環境下ではHIF1αが増え、髄鞘が作られやすくなることが明らかになった。
さらにHIF1αの生体内での役割を調べたところ、神経傷害後の再生においては、HIF1αを欠損するマウスでは再生が少し遅れて進行することがわかった。そこで、マウスの末梢神経傷害モデルに対して、HIF1αの分解を阻害する薬物を投与すると、傷害からの回復が促進された。このことから、HIF1αが少ないと神経の回復が遅れることが判明した。
低酸素状態でHIF1αが神経の再生を助けていると判明
HIF1αがシュワン細胞でどのような遺伝子の転写を制御することによって髄鞘形成を制御しているのかを検討したところ、Myelin basic protein(MBP)やEgr2など髄鞘化に必須とされる遺伝子をはじめとする髄鞘化との関連が報告されている複数の遺伝子の制御を行っていることを確認。HIF1αが髄鞘作りに必要な遺伝子の働きをコントロールしていることがわかった。
これらの結果から、HIF1αはシュワン細胞において低酸素に応答して髄鞘化関連遺伝子の発現制御を行うことにより、特に神経再生の局面において、髄鞘化促進的に作用していることが明らかとなった。つまり、低酸素状態ではHIF1αが神経の再生を助けていることが判明した。
発見したメカニズムを神経再生促進に応用するためには、さまざまな検討が必要
今回の研究により、神経組織中の比較的小さな酸素濃度の変動が、HIF1αの機能を介して神経系の再生に重要な影響を与える可能性が示された。
「このような仕組みは、神経損傷時の環境下で神経再生を進めるために生体が獲得したメカニズムなのかもしれない。今後このメカニズムを神経再生促進に応用するためには、さまざまな検討が必要だ」と、研究グループは述べている。
▼関連リンク
・国立精神・神経医療研究センター トピックス



