軟部組織に異所性骨化が生じる希少難病
京都大学iPS細胞研究所(CiRA)は5月27日、進行性骨化性線維異形成症(FOP)において、治療タンパク質の局所送達とラパマイシンの併用によって異所性骨化の進行抑制効果が高まることを動物モデルで確認したと発表した。この研究は、同研究所のPan Gao研究員、池谷真准教授(CiRA臨床応用研究部門)らの研究グループによるもの。研究成果は、「JBMR Plus」にオンライン掲載されている。
画像はリリースより
(詳細は▼関連リンクからご確認ください)
FOPは、筋肉をはじめとする軟部組織内で異常な骨形成が進行する難治性骨疾患で、患者QOLを著しく低下させる。十分な効果が得られる治療法がいまだに開発されておらず、新たな治療戦略が求められている。
研究グループはこれまでに、FOPの異所性骨形成に対して「ラパマイシン」が進行抑制効果を持つことを明らかにしている。ラパマイシンは、臓器移植における拒絶反応の防止などに使われている免疫抑制剤で、細胞内ではmTORの活性を阻害する効果がある。
また、同グループは骨形成タンパク質阻害物質「ACVR2B-Fc」をiPS細胞から作製した誘導間葉系間質細胞(iMSC)に搭載することで、効率的に標的組織へ届ける方法を開発している。ACVR2B-Fcは、FOPの増悪因子の一つであるBMPタンパク質の受容体の細胞外部分に、抗体の定常領域の一部であるFc領域を融合したタンパク質。偽受容体として機能するため、BMPによって引き起こされるシグナルを止める働きがある。Fcと融合することにより、血液中で分解される速度が遅くなることが期待される。
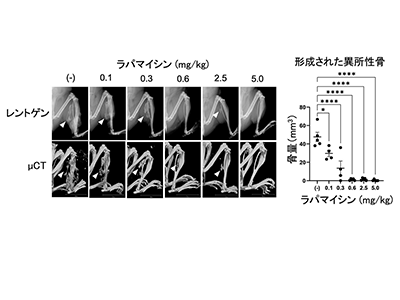
ラパマイシンが用量依存的にモデルマウスの異所性骨を抑制
そこで今回の研究では、FOP進行抑制剤としてのラパマイシンと、iMSCを活用したACVR2B-Fcを患部に送達する技術の併用による治療効果の向上を目指した。
まず、FOPモデルマウスに対してラパマイシンの濃度を変化させて単独で投与し、その効果を検証した。その結果、ラパマイシンの投与量依存的に異所性骨抑制効果が変化することを確認した。
ラパマイシン併用がACVR2B-Fcの骨化抑制効果を増強
次に、ACVR2B-Fcを搭載したiMSCを動物モデルへ移植した。さらに低用量ラパマイシンを併用投与したところ、単独治療と比較して異所性骨化抑制効果が増強されることが示された。
併用療法は外科的切除後の再発も抑制
さらに、一次骨化(初発病変)の後に外科的に異所性骨を切除し、その後の再発(二次骨化)を観察するモデルにおいても同様に、併用療法に再骨化抑制効果があることを確認した。また、ラパマイシンの併用はiMSCの局所での生存と機能維持に寄与していることを示唆するデータも得た。
以上の結果から、iMSCによる治療タンパク質の局所送達とラパマイシンの併用が、FOPの一次骨化だけでなく、外科的切除後の二次骨化の抑制にも有効である可能性が示された。
FOPの新たな治療戦略として期待、今後も検討を継続
同研究は、FOPに対する新たな治療戦略として、iMSCを利用したACVR2B-Fc融合タンパク質の局所送達とラパマイシンの併用療法が有効であることを明らかにした。これまで困難とされてきた外科的切除後の再発(二次骨化)に対しても、骨化抑制効果が認められたことは意義がある。これらの成果から、FOPのみならず、他の異所性骨化疾患や再生医療分野にも応用可能な新しい細胞・分子ハイブリッド治療の基盤となることが期待される。
「今回の実験結果によれば併用療法の再骨化に対する効果は限定的であり、完全に抑制されるまでの効果は発揮できていない。他の治療薬との組み合わせ、投与経路、投与量など、さらなる戦略の検討が必要と考えられる」と、研究グループは述べている。
▼関連リンク
・京都大学iPS細胞研究所(CiRA) ニュース・イベント



