CIDPと類縁疾患で検出される自己抗体を測定する体外診断用医薬品
九州大学は6月3日、自己抗体測定キット「NF155抗体「ヤマサ」EIA」および「CNTN1抗体「ヤマサ」EIA」が2025年5月12日付で体外診断用医薬品として承認されたと発表した。この研究は、同大大学院医学研究院の磯部紀子教授、同大病院脳神経内科の緒方英紀助教らとヤマサ醤油株式会社の共同研究グループによるもの。
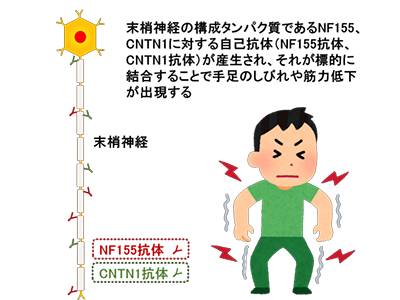
画像はリリースより
(詳細は▼関連リンクからご確認ください)
慢性炎症性脱髄性多発神経炎(chronic inflammatory demyelinating polyneuropathy:CIDP)は、後天性の脱髄性末梢神経障害の代表的疾患。2か月以上にわたって進行または再発を繰り返す経過をたどり、四肢の筋力低下やしびれ感をきたす末梢神経の疾患である。近年、一部のCIDP症例で、neurofascin 155(NF155)やcontanctin 1(CNTN1)抗体が陽性になることが明らかとなった。治療反応性の違いや自己抗体の存在などから、自己免疫性ノドパチーと命名され、CIDPの類縁疾患として扱われることとなった。NF155抗体やCNTN1抗体は自己免疫性ノドパチー症例で検出される自己抗体である。
多施設共同臨床性能試験で示された有用性に基づく承認
今回承認された同自己抗体測定キットは、enzyme immunoassay(EIA)法により血清中のNF155抗体あるいはCNTN1抗体を測定し、CIDP並びに自己免疫性ノドパチーの診断補助をすることを目的としている。
承認取得のため、九州大学をはじめとした全国4施設で「IgG4自己抗体陽性慢性炎症性脱髄性多発神経炎に対する抗ニューロファシン155抗体測定用ELISAキットおよび抗コンタクチン1抗体測定用ELISAキットの有用性評価のための多施設共同臨床性能試験」が実施された。同試験で示された有用性に基づき、ヤマサ醤油株式会社より体外診断用医薬品の製造承認申請を医薬品医療機器総合機構へ提出し、この度の承認に至った。今後は、日常診療で広く利用可能となるよう、保険適用に関する手続きを進める予定、と研究グループは述べている。
▼関連リンク
・九州大学 プレスリリース



