骨格筋幹細胞の臨床応用、非生体由来の細胞外マトリックスと高効率な分化誘導が課題
京都大学iPS細胞研究所(CiRA)は5月7日、ヘパラン硫酸鎖が結合した次世代型合成細胞外マトリックスを開発し、iPS細胞の分化誘導に用いることで、高効率に骨格筋幹細胞を分化誘導できることを見出したと発表した。この研究は、CiRA臨床応用研究部門の超明明特定研究員(研究当時、現:重慶医科大学基礎医学院教授)、大阪大学蛋白質研究所の関口清俊寄附研究部門教授、CiRA臨床応用研究部門の櫻井英俊准教授らの研究グループによるもの。研究成果は、「Advanced Science」にオンライン掲載されている。
画像はリリースより
(詳細は▼関連リンクからご確認ください)
筋ジストロフィーに対する再生医療の研究開発として、櫻井准教授らの研究グループはこれまでに、ヒトiPS細胞から高い再生能を持つ骨格筋幹細胞の誘導に成功している。しかしこの報告で用いられた分化誘導方法は、臨床応用を目指すにあたって二つの問題点があった。一つは誘導効率が低いことであり、実際に移植する量の骨格筋幹細胞を得るために、相当量の細胞を準備する必要があり、製造コストが懸念される。もう一つは、培養ディッシュのコーティング剤に生体由来の細胞外マトリックスである「マトリゲル」を使用していることであり、ヒトに移植する細胞を製造するためには、生体材料由来ではなく合成タンパク質を使うことが望まれる。
開発した次世代型ラミニンE8フラグメント、骨格筋幹細胞の分化誘導効率を有意に上昇
これらの問題点を解決するため、合成細胞外マトリックスの専門家である関口教授と今回の研究グループを形成した。関口教授らは、これまで基底膜の細胞外マトリックスであるラミニンの細胞接着活性をほぼ100%保持した組換えラミニンE8フラグメントを開発し、この組換えフラグメントはiPS細胞の維持培養などに広く用いられている。さらに、マトリゲルの機能を模倣するため、パールカンという細胞外マトリックスのヘパラン硫酸鎖担持ドメインをラミニンE8フラグメントに連結した「次世代型ラミニンE8フラグメント」を開発し、今回の研究材料としてiPS細胞から骨格筋幹細胞への分化誘導に応用した。
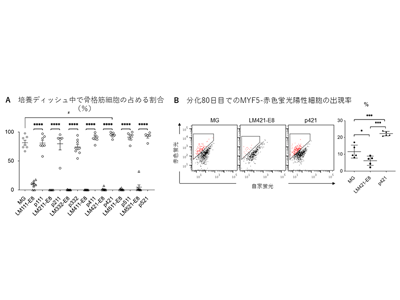
研究グループは、まず全ての種類のラミニンE8フラグメントと次世代型ラミニンE8フラグメントを用いて、骨格筋幹細胞分化誘導を実施し、中間段階の分化38日目で骨格筋細胞への分化誘導効率を評価した。すると従来のラミニンE8フラグメントでは全て骨格筋細胞への分化が見られないのに対し、次世代型ラミニンE8フラグメントでは全てがマトリゲル(MG)と同等かそれ以上の骨格筋細胞誘導能を持つことがわかった。その中でも次世代型ラミニン421E8フラグメント(p421)が統計学的有意に誘導効率を上昇させたことから、以降の実験ではp421をラミニン421E8フラグメント(LM421-E8)と比較して実験を進めた。骨格筋幹細胞のマーカーであるMYF5遺伝子が発現すると赤色蛍光を発するiPS細胞を用いて、骨格筋幹細胞への分化誘導を実施し、分化80日目で赤色蛍光を発する細胞(=骨格筋幹細胞)を計測した。従来法のMGでは平均12%程度の誘導効率、LM421-E8では平均6%程度と半減したのに対し、p421では平均22%程度の誘導効率に上昇した。
次世代型ラミニン421E8フラグメントは最も初期から沿軸中胚葉の分化誘導を促進
次に、骨格筋幹細胞誘導効率の上昇が、どの時点で起きているかを検証した。骨格筋幹細胞誘導の最初のステップは沿軸中胚葉の誘導であるので、初期中胚葉マーカーのBRACHYURY(T)および沿軸中胚葉マーカーのTBX6の発現を免疫染色で確認した。分化2日目のTの発現はMGでは比較的均一に発現しており、LM421-E8では一部にしか発現していなかった。p421ではMGに比べて輝度が高く発現していた。分化4日目のTBX6の発現は、MGでは球形の細胞塊にはある程度発現しているものの、TBX6が発現していない細胞がその周囲に広がる傾向が観察された。LM421-E8ではTと同じく、ごく一部の細胞のみで発現するにとどまった。一方でp421では球状の細胞塊のみが特異的に誘導される傾向が確認され、ほとんどすべての細胞が陽性だった。以上より、p421は分化の最も初期において沿軸中胚葉の誘導効率を上昇させていることが明らかとなった。さらに、その効果を生み出す時期が分化7日目までであることを見出した。
ヘパラン硫酸鎖がFGFシグナルを効率よく伝え中胚葉分化を促進
続いて、p421の持つ中胚葉分化促進効果が、どのようなメカニズムで起きるのかを検証した。まずヘパラン硫酸の拮抗薬であるSurfenを分化誘導の開始時および分化2日目から添加すると、MGコート上でもp421コート上でも中胚葉分化マーカーであるTおよびTBX6の発現がそれぞれ低下した。このことから、ヘパラン硫酸が中胚葉分化を促進する機能を持っていることがわかった。
ヘパラン硫酸鎖は、成長因子と呼ばれるホルモンの一種を捕捉してそのシグナルを細胞に効率よく伝える役割を担っている。そこで、次世代型ラミニンE8フラグメントがおそらくは何らかの成長因子を捕捉して効果を発揮しているのではないかと仮説を立てた。そこでSurfen添加と同じタイミングでさまざまな成長因子の阻害剤を添加したところ、FGF受容体の阻害剤は全て強力にT発現についてもTBX6発現についても抑制し、中胚葉誘導が阻害されていることがわかった。これらの結果から、p421に結合しているヘパラン硫酸鎖によりFGFシグナル伝達がFGF受容体に効率よく伝わることが、中胚葉分化促進効果のメカニズムであることが明らかとなった。
分化誘導開始前の維持培地に添加されるbGFGがFGFシグナルを伝えていた
しかし、分化誘導培地にFGFは添加しておらず、どこからFGFシグナルが伝えられているのか不明だった。研究グループは、分化誘導開始前に使用しているiPS細胞維持培地であるAK02Nには100ng/mlという比較的高用量のbFGFが添加されていることに気が付き、このbFGFがヘパラン硫酸鎖に捕捉され、分化誘導開始以後にも作用しているのではないかと仮説を立てた。そこで、まずAK02Nに含まれるbFGFの量を段階的に減らす実験を行った。するとbFGFの濃度を5ng/mlまで減らした際に、分化2日目のTの発現量が大きく低下し、やはり分化誘導開始前のbFGFが、その後の中胚葉分化促進効果に影響を与えることがわかった。次に、その効果はFGF受容体を介するものかどうかを検証するため、さまざまな成長因子の阻害剤を分化誘導1日前から開始時まで添加して、分化2日目のTの発現を解析した。結果は分化誘導後の際と同じく、FGF受容体阻害剤を阻害した際に強力にTの発現が抑制され、やはり分化誘導開始前にbFGFからFGFシグナルが伝えられていることが重要であることがわかり、そのためにはヘパラン硫酸鎖によるbFGFの捕捉が機能しているであろうと考えられた。
ヘパラン硫酸鎖の結合位置が分化誘導効率に重要
分化誘導開始前のbFGFの添加が重要であると判明したことから、研究グループはp421のようにヘパラン硫酸鎖を持たないLM421-E8でも、単純にbFGFを過剰量添加すれば中胚葉分化促進効果を見出せるのではないかと考え、bFGFの大量添加実験を行った。LM421-E8でコートしたプレート上で分化誘導を実施し、分化誘導3日前から開始時まで100、500、1000ng/mlという大量のbFGFを添加した。しかし、大量のbGFG添加によりT発現量は上昇したものの、p421を用いた条件には遠く及ばなかった。
やはりヘパラン硫酸鎖が必要であるということがわかったため、次にヘパラン硫酸鎖を結合する位置によって違いがあるのか、どこに付けても効果があるのかを検証した。通常のp421ではヘパラン硫酸鎖はラミニンα鎖のC末端に連結されているが、ヘパラン硫酸鎖をβ鎖のN末端あるいはγ鎖のN末端に連結した次世代型ラミニンE8フラグメントを作製し、中胚葉への分化誘導効率を比較検討した。その結果、C末端に結合させた通常のp421が最も効果が高いことが明らかとなった。C末端側は、細胞が実際に接着する場でもあり、接着した細胞膜表面に近い位置にヘパラン硫酸鎖が存在することで、効率よくFGFシグナルを伝えられている可能性が示唆された。
骨格筋幹細胞分化誘導の効率化、筋疾患の病態解明や創薬研究にも貢献すると期待
今回の研究では、次世代型ラミニンE8フラグメントであるp421を用いることで、ヒトiPS細胞からの骨格筋幹細胞分化誘導効率を上げることに成功した。これまで用いていたネズミ腫瘍由来の「マトリゲル」は、再生医療の臨床応用には適さないため、ヒト由来の組換えタンパク質であるp421の使用により高効率で骨格筋幹細胞を分化誘導できることは、ヒトに投与可能な骨格筋幹細胞分化誘導プロトコール確立に寄与する。またヘパラン硫酸鎖により初期の中胚葉への誘導分化効率を上昇させることが、最終的な骨格筋幹細胞分化誘導効率を上げることがわかり、今後の分化誘導プロトコールの安定化や改良に役立つ知見を多く得ることができた。
「iPS細胞由来骨格筋幹細胞は、患者由来のヒトiPS細胞を用いることで、病態研究や創薬スクリーニングにも応用可能である。効率の良い分化誘導法により筋疾患の病態解明や創薬研究にも貢献することが期待される」と、研究グループは述べている。
▼関連リンク
・京都大学iPS細胞研究所(CiRA) ニュース



