腸管病原性大腸菌の排除メカニズムの全容は不明
京都大学は1月11日、腸管病原性大腸菌の排除の起点となる炎症性サイトカインの一つ「インターロイキンー23(IL-23)」を産生する樹状細胞の一群を発見したと発表した。この研究は、同大医生物学研究所の廣田圭司准教授、小原乃也同博士課程学生、近藤玄同教授、渡邊仁美同助教らの研究グループによるもの。研究成果は、「Journal of Experimental Medicine」にオンライン掲載されている。
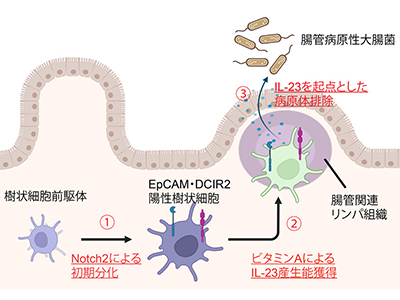
画像はリリースより
(詳細は▼関連リンクからご確認ください)
腸管病原性大腸菌は腸炎の原因菌の一つ。日本でも乳幼児の集団感染が報告されており、乳幼児や高齢者が重篤な症状や死亡に至るケースも少なくない。この感染症の予防法・治療法、特に重篤化を防ぐ方法を確立するためには、病原菌の排除に特化した腸管免疫反応を理解することが重要となる。しかし、腸管病原性大腸菌の排除メカニズムの全容は明らかになっておらず、特にどのような細胞が病原菌を認識し、排除の反応を開始するのかは不明だった。
IL-23レポーターマウスを作製し、産生細胞を解析
研究グループは、腸管病原性大腸菌に対する免疫応答の起点となるサイトカインIL-23に注目した。IL-23は免疫細胞が腸管病原性大腸菌を認識した初期に分泌されるサイトカインだ。このサイトカインを作れないマウスはこの病原菌を排除できず、感染による症状が重症化することがわかっている。このIL-23を産生する免疫細胞がどのような種類の細胞で、どのような性質を持っているのかを明らかにすることができれば、腸管病原性大腸菌の排除反応がどのように始まるのかも明らかにできると考えた。
研究グループはIL-23を産生する細胞を可視化するツールであるIL-23レポーターマウスの作成に成功。このIL-23レポーターマウスに腸管病原性大腸菌を感染させ、どのような細胞がIL-23を産生しているかを解析した。
IL-23を多量に産生する新たな樹状細胞集団を同定、EpCAM+DCIR2+CD103-CD11b-
その結果、腸管の免疫細胞のうちIL-23産生に特化した樹状細胞の一部を発見した。樹状細胞にはさまざまな種類が存在することが報告されている。そこで、どのような種類の樹状細胞がIL-23を産生するかを調べるために、表面抗原に対する抗体約260種類を用いて表面抗原スクリーニングを行ったところ、今までに報告された腸管樹状細胞とは異なる表面抗原を持つ樹状細胞がIL-23を産生していることが判明した。
新たに発見されたIL-23産生細胞は、細胞表面上のタンパク質であるEpCAMとDCIR2が共陽性かつCD103とCD11bが陰性の表面抗原を持つ樹状細胞だったという。
腸管病原性大腸菌を排除する起点として「腸管関連リンパ組織」が重要
次に、IL-23を産生する樹状細胞が腸管のどのような場所に存在するのかを調べた。免疫細胞の大部分は腸管の絨毛や陰窩に分布する一方で、特殊な構造である腸管関連リンパ組織という免疫細胞の集塊が存在することも明らかになっている。そこで、組織透明化技術を用いて腸管全体を観察し、IL-23産生樹状細胞の分布を調べた。
結果、その大部分は腸管関連リンパ組織に存在することが明らかになった。これは、腸管病原性大腸菌を排除する起点として腸管関連リンパ組織が重要な免疫器官であることを示唆している。
IL-23産生樹状細胞の発生に、Notch2とビタミンAの刺激が重要と判明
最後に、IL-23産生樹状細胞が生体内でどのように発生するのかを調べた。IL23産生樹状細胞とその他の樹状細胞の遺伝子発現の比較から、Notch2およびビタミンAによる刺激がIL-23産生樹状細胞の発生に重要であると仮説を立てた。その仮説を検証するため、それぞれのシグナル経路を遮断し、IL-23産生樹状細胞の発生・分化に影響があるか調べた。
その結果、Notch2シグナルが遮断されたマウスでは、IL-23産生細胞を含むEpCAM・DCIR2共陽性の樹状細胞がほぼ全て消失していた。一方で、ビタミンAシグナルが遮断されたマウスでは、EpCAM・DCIR2共陽性の樹状細胞は正常通り存在するものの、これらの細胞のIL-23産生能力が著しく低下していた。
以上より、腸管のIL-23産生樹状細胞は(1)Notch2シグナルによって樹状細胞前駆体からEpCAM・DCIR2共陽性樹状細胞に分化、(2)ビタミンAシグナルによって未熟なEpCAM・DCIR2共陽性樹状細胞が成熟し、IL-23の産生能力を獲得、(3)腸管関連リンパ組織に分布したIL-23産生樹状細胞が腸管病原性大腸菌を認識すると、多量のIL-23を分泌することで病原菌を排除する、という流れで腸管病原性大腸菌の排除を行っていることが明らかになった。
自己免疫疾患を抑制する新しい治療法の確立を目指す
発展途上国の乳幼児におけるビタミンA欠乏症が腸管病原性大腸菌感染の重篤化を招くということが疫学研究によって証明されているものの、ビタミンAが病原菌の排除に重要である理由を明らかにした免疫学的研究は一部に留まる。今回の研究では、腸管病原性大腸菌の排除の起点となるIL-23産生樹状細胞の分化にビタミンAの代謝物が非常に重要であることを明らかにされた。これは、大腸菌感染に対するビタミンAの重要性の一部を説明する成果と考えられる。また、研究グループの実験システムを使用することで、ビタミンA以外にも、どのような栄養素がIL-23産生樹状細胞の機能に重要なのか調べることが可能となり、腸管病原性大腸菌感染症の重篤化予防に役立てることができる。
今回の研究の最も大きな成果の一つはIL-23レポーターマウスの開発に成功し、IL-23産生細胞の可視化を可能にしたことだ。IL-23が感染防御に関わっている他の重篤な感染症として、結核が挙げられる。さらにIL-23が過剰に産生されると潰瘍性大腸炎、クローン病、乾癬などの自己免疫疾患が引き起こされる。IL-23レポーターマウスはこれらの感染症や自己免疫疾患において、どのような細胞がIL-23を産生し、どのように病気を制御しているのかを調べるための極めて強力なツールになり得る。最終的にはIL-23産生細胞を操作することで、腸管病原性大腸菌や結核に対する抵抗性を高める、自己免疫疾患を抑制するといった新しい治療方法の確立を目指したい、と研究グループは述べている。
▼関連リンク
・京都大学 最新の研究成果を知る



