膵がん
膵がんは、消化器がんのなかで最も予後不良のがんである。膵臓は胃の裏側に位置し、十二指腸とくっついていて、脾臓まで横に細長くなっている後腹膜の臓器であるため、早期発見が困難であり、たとえば2 cm以下の小さながんであっても、すぐに周囲への浸潤や、近くのリンパ節への転移、肝臓などへの遠隔転移を伴うことが多い、悪性度の高いがんである。
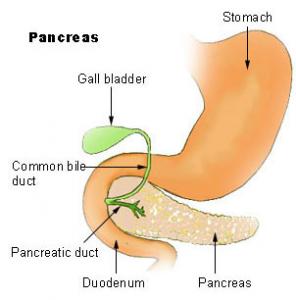
(画像はウィキメディアより)
切除後の補助化学療法に関する第3相試験結果
大鵬薬品工業は、膵がん切除後の補助化学療法における塩酸ゲムシタビン(療法とS-1(以下TS-1)療法の第3相比較試験の結果を発表した。本試験は、33施設において、膵がん切除後(UICC stage II以下、もしくは腹腔動脈合併切除を施行したstage III)の患者385例を、塩酸ゲムシタビン単独投与群と、経口抗がん剤であるTS-1単独投与群の2つの群に割り付けた。主要評価項目は全生存期間で、塩酸ゲムシタビン単独投与群は、1,000 mg/m2の塩酸ゲムシタビンを1日目、8日目および15日目に点滴静注し、22 日目は休薬する28 日を1コースとし、6ヶ月間投与した。 TS-1 単独投与群は体表面積に合わせて規定された投与量(80 mg、100 mg、12 0mg/日)を1日2回、28日間連続経口投与し、その後14日間休薬する42日を1コースとし、4コース(6ヶ月間)まで実施した。
その結果、膵がん切除後の補助化学療法としての標準治療薬である塩酸ゲムシタビン単剤に対して、TS-1単剤の全生存期間における優越性が証明され、TS-1が生存期間を大幅に延長させることを示した。(堤朝子)
▼外部リンク
大鵬薬品 ニュースリリース 2013年1月28日
http://www.taiho.co.jp/2013/20130128.html








