米国ではすでに50種類以上の臨床開発が進む抗体薬物複合体
国立がん研究センターは5月9日、質量顕微鏡を用いて、抗体薬物複合体(ADC)のがん組織中の薬物放出・分布を可視化した、世界初の評価方法を確立したと発表した。この研究は、同先端医療開発センター新薬開発分野と理化学研究所、株式会社島津製作所の研究グループが共同で行ったもの。研究成果は、英科学誌Nature系オンライン科学誌「Scientific Reports」に4月21日付けで掲載されている。
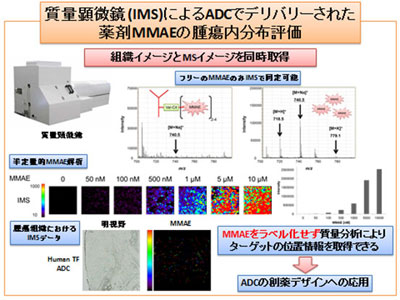
画像はリリースより
ADCは、抗体に抗がん剤などの薬を付加したもの。抗体が特定の分子をもつがん細胞に結合する性質を利用して、薬を直接がん細胞まで運び、そこで薬を放出することで、抗腫瘍効果を発揮する。抗体によってがん細胞に標的を絞り、かつ正常な細胞への影響を避けるという目的で設計された、新しいタイプのがん治療薬だ。海外、特に米国ではすでに50種類以上のADCの臨床開発が進められており、将来、多くのADCが日本にも導入されることが予想される。
さらに、トラスツズマブに抗がん剤を付加したADC(T-DM1、トラスツズマブ エムタンシン)がトラスツズマブで効果が得られなくなったHER2陽性進行・再発乳がんに対して有効であることが明らかになったことから、抗体薬の耐性の問題を克服する新たな手段としても大きな期待が寄せられている。
その一方で、ADCが抗腫瘍効果を発揮するための必須条件である「ADCががん細胞に到達する」「がん細胞中で薬を放出する」という2点を正確に評価する方法がなく、ADCの創薬デザインにおいては至適な設計がなされていなかった可能性があるという。
これまでADCの体内動態をみるには、付加した薬を放射性同位元素で標識(ラベル)する必要があったが、この方法ではコストが高く、時間もかかる。また、薬を放出する前と、放出された後の状態を見分けることができず、ADCが本当にがん細胞に到達しているのか、さらにそこで薬が放出されているのかまでは評価できていなかった。
次世代のがん治療薬と期待されるADCの精巧な設計を可能に
今回、研究グループは、島津製作所が開発した質量顕微鏡を用いて、がん組織中におけるADCからの薬物の放出を直接みることに成功。この手法を用いると、ADCから放出された薬剤を明確に同定することができ、放出された薬がどこにどの程度分布しているかを定性的かつ半定量的に分析することが可能だという。さらに、薬を放射性同位元素でラベルすることなく評価できるため、従来の方法に比べて正確ながん細胞への薬剤の分布がわかるだけでなく、コストや簡便性の点でも優れているとしている。
また、血管外に漏れ出した血液の凝固反応が、がん細胞の表面や腫瘍血管および周囲の組織因子(TF)の発現によって起こることに着目。その組織因子に対する抗体を樹立したという。その抗体に理化学研究所で作製したリンカーでMMAEという薬を付加したADC(抗TF抗体-MMAE複合体)を作製。このADCを担がんマウスに静脈注射し、ADCががん組織に運ばれ、MMAEががん組織中のがん細胞のかたまりのところで特異的に放出されていることを質量顕微鏡で確認したとしている。
ADCの研究開発は、今後さらに活発化することが予測される。同研究で確立した腫瘍内薬剤分布の評価方法は、ADCががん組織に到達し、付加薬物ががん細胞まで送達される至適な条件を導き出すにあたって、きわめて簡便かつ正確な方法といえるため、今後ADCの精巧な設計のためには欠かせない手法のひとつとして期待が寄せられる。
▼関連リンク
・国立がん研究センター プレスリリース



