IPFは高率に肺がんを合併、合併すると極めて予後不良
東京慈恵会医科大学は3月1日、加齢とともに発症率が高まる肺疾患である特発性肺線維症(idiopathic pulmonary fibrosis:IPF)に高率に合併する肺がんの悪性化に関わる要因が、IPFの病態において重要な老化した線維芽細胞が分泌するエクソソーム(細胞外小胞)により促されていることを発見したと発表した。この研究は、同大エクソソーム創薬研究講座の藤田雄講師、内科学講座呼吸器内科の藤本祥太助教、荒屋潤教授、桑野和善講座担当教授、外科学講座呼吸器外科の大塚崇講座担当教授、東京医科大学医学総合研究所分子細胞治療研究部門の落谷孝広教授らの研究グループによるもの。研究成果は、「American Journal of Respiratory Cell and Molecular Biology」にオンライン掲載されている。
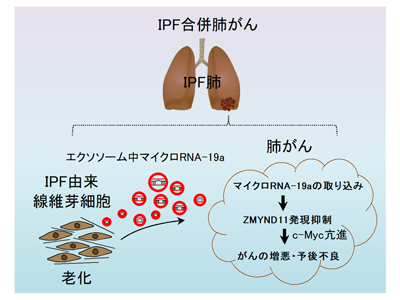
画像はリリースより
(詳細は▼関連リンクからご確認ください)
IPFは、慢性かつ進行性の線維化に伴う呼吸機能低下と呼吸苦を呈する、原因不明の難病疾患である。国内では、約1万3,000〜1万5,000人の患者がいると言われているが、初期や早期は自覚症状のないケースもあり、潜在的な数はそれ以上と考えられている。またIPFは、加齢とともにその発症率が上昇する老化関連肺疾患であり、IPF肺では老化した気道上皮細胞や線維芽細胞が多く存在し、これらが老化関連分泌因子(SASPs)の分泌を介して組織修復遅延や慢性炎症を誘導し病態増悪につながることが、昨今の研究からわかってきた。IPFは、診断後の平均生存期間が3~5年と短く、治療薬は抗線維化薬であるピルフェニドンとニンテダニブの2剤が臨床現場で使用されているが、いまだに予後が不良な疾患として知られている。さらに、IPFでは高率に肺がんを合併することが知られており、がんの合併したIPF患者の予後は極めて不良であることが報告されている。
エクソソームは脂質二重膜に囲まれた100nm前後の細胞外小胞で、マイクロRNAやタンパク質など多彩な分子を内包し、組織修復や再生、疾患の発症や進展など、多くの機能や病態に関与することが知られている。研究グループは、IPFにおいてその病態進展に関与する線維芽細胞に着目し、それらから分泌されるエクソソームによる肺がんへの影響を解析し、IPF自身や合併する肺がんに対する新たな治療戦略となる研究を目指した。
IPF由来の線維芽細胞は老化が進行、分泌するエクソソームはがん細胞の増殖を促進
IPF患者およびnon-IPF患者に由来するヒト手術肺検体から線維芽細胞(LFs)を分離培養した。IPF患者由来の線維芽細胞(IPF-LFs)とnon-IPF患者由来の線維芽細胞(nonIPF-LFs)を比較検討したところ、IPF-LFsは肺の線維化病態形成および進展に重要な線維芽細胞から筋線維芽細胞への分化形質を有しており、さらに細胞老化がnon IPF-LFsよりも有意に誘導されていることが判明した。この筋線維芽細胞化および老化の形質をもつIPF-LFsの分泌するエクソソームの機能を詳細に解析するために、超遠心法でエクソソームを回収した。これらエクソソームを肺がん細胞株であるA549およびH460細胞に添加したところ、IPF-LF由来エクソソームは有意にがん細胞の増殖を促進させることを見出した。
エクソソーム中のマイクロRNA-19aが肺がん増殖に重要
老化したIPF-LF由来エクソソームによる肺がん増殖促進のメカニズムを検討した。エクソソームは多彩な分子を内包し複数のメカニズムで作用する。そこで、IPF-LF由来エクソソームに含まれる分子を検討した。網羅解析などの結果、内包物の中でも特にマイクロRNA-19aが、肺がん細胞の増殖において重要であることが判明した。マイクロRNA-19aはこれまでの報告などからも、肺がん細胞で有意に発現が増加するがん関連マイクロRNAであり、がんゲノムデータベースであるThe CancerGenome Atlas(TCGA)を用いた解析においても、肺がんの予後に関わる重要な因子であることがわかった。
マイクロRNA-19a<ZMYND11抑制<c-Myc活性化<肺がん悪性化
IPF患者由来線維芽細胞が分泌するエクソソーム中のマイクロRNA-19aが、肺がん細胞に取り込まれたのち、どのようなメカニズムでがんの悪性化が誘導されるのか探索した。網羅解析などの結果から、マイクロRNA-19aはZMYND11という遺伝子を直接抑制制御していることが判明した。ZMYND11はヒストンの修飾部位と結合し、転写伸長に関与する因子であり、下流のがん遺伝子の転写抑制に関与していることが報告されている。実際に肺がん腫瘍サンプルでZMYND11の発現を評価してみると、IPFに合併した肺がんではZMYND11の発現は低下していることもわかった。さらに、ZMYND11は、複数のがん遺伝子を制御しており、特にc-Mycというがん遺伝子の発現が、マイクロRNA-19a/ZMYND11の経路で活性化され肺がん悪性化に関与することが判明した。
さまざまな臓器線維症に合併するがんの悪性化メカニズム解明にもつながることを期待
研究グループは、IPFに合併する肺がんの予後が悪い要因として、老化したIPF患者由来線維芽細胞が分泌するエクソソームによって促されていることを突き止めた。IPF患者由来線維芽細胞が分泌するエクソソーム自身、または内包するマイクロRNA-19aを阻害することは、IPFの病態のみならず、合併する肺がんの悪性化制御にもつながる新しい治療戦略となる可能性がある。「この知見は、肺疾患のみならず、さまざまな臓器線維症に高頻度に合併する多様ながんの悪性化メカニズムの解明にもつながる。今後、さまざまな臓器に認められる線維化病変とがんとのつながりを解析することにより、新たながん治療への応用が期待される」と、研究グループは述べている。
▼関連リンク
・慈恵大学 プレスリリース








