脳細胞間のpH測定は予防や治療につながるが、既存測定技術は分解能など課題
東北大学は12月21日、生体埋め込み型の新しいpH可視化プローブを開発し、脳内の複数点においてpH変化を同時に高感度で測定することを可能にし、世界で初めて、脳深部の海馬において、疼痛刺激に伴うpHの微小変化をリアルタイムで補捉することに成功したと発表した。これは同大学際科学フロンティア研究所郭媛元助教(医工学研究科・医学系研究科兼務)、医工学研究科の吉信達夫教授、医学系研究科の虫明元教授らの研究グループによるもの。研究成果は、「Biosensors and Bioelectronics」に掲載されている。
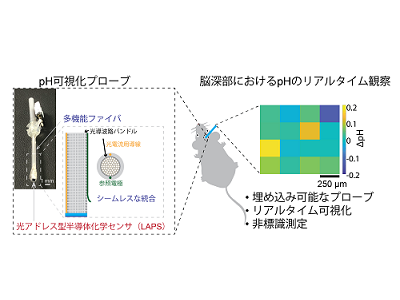
画像はリリースより
脳の中には、神経細胞やグリア細胞があり、複雑な回路が形成され、さまざまな信号が細胞間で伝達されている。脳回路の中で、神経細胞が電気活動していることを記録する技術はすでに成熟している。しかし、脳内の細胞間コミュニケーションを担っているのは繊細な化学信号であり、その活動を観察する技術は今のところ、細胞や組織を蛍光標識する必要がある光学的なイメージング法に限られている。それゆえ、脳内で化学信号を高感度かつ非標識で記録できる新たな技術が必要とされていた。
さまざまな化学信号のうち、pH(水素イオン濃度)は脳の恒常性を維持するために、ある一定の範囲内で厳密に調節されている。もし脳細胞周辺でpHがその範囲を大きく超えてしまうと、脳の異常活動を引き起こしてしまうことから、てんかん、脳虚血、うつ病などの病気との関連が指摘されている。脳細胞間のpHコミュニケーションを動的に可視化できれば、pHと脳活動の関連や、病気のメカニズムの解明および予防・治療につながっていくと期待される。
既存の主な生体内pH測定技術は以下のようにまとめられる。核磁気共鳴画像法を用いた生体内pH測定法は、時間・空間分解能が低いため、脳内で起こっている細胞レベルの活動を観察することが難しいという問題がある。また、電気化学的原理に基づくpH電極は、極めて局所の計測に限られてしまう。光学的なイメージング法では、細胞や組織を蛍光標識することが必要となり、生体本来の活動を妨げる可能性があるうえ、光学顕微鏡下での観察となるため、測定対象の動物は固定されたままとなり、行動との因果関係を調べる場合の制限となる。これらを踏まえ、生体埋め込み型で、時間・空間分解能が高いイオン可視化ツールの新たな開発が重要と考えられた。
LAPSと多機能ファイバの複合化で、オールインワンプローブ型イオン可視化ツールを実現
研究では、イオン濃度の分布を可視化できる半導体化学イメージセンサと、多機能ファイバ技術を組み合わせることによって、新しい生体埋め込み型のpH可視化プローブを実現した。化学イメージセンサは「Light-addressable potentiometric sensor」(LAPS)と呼ばれる半導体センサの原理を利用した。LAPSは半導体基板上にイオン感応面となる絶縁層を形成した構造を持ち、イオン濃度の空間分布に対応して、センサ面上に電位の分布が生じる。その結果、電界効果によって半導体中に生じる空乏層の静電容量が各点ごとに異なるため、各点を変調光で照射して得られる光電流を計測することによって、イオン濃度分布を画像化することができる。
平面構造を持つLAPSは、そのままでは生体内に埋め込むことが困難だった。この課題を解決するため、必要な構造や機能を自在に組み合わせたプローブを作製することができる熱延伸技術を活用し、LAPSの生体内の応用に必要な光導波路バンドル・導線・参照電極などの機能を集積した複合プローブを開発した。この方法は「金太郎あめ」を作る方法と似ており、まず集積したい各要素を束ねた成形物(〜20mm)を作製し、これを加熱しながら引き伸ばすことによって、内部の幾何学的構造を維持したまま、直径が数百ミクロンのプローブを作製することができる。さらに、LAPSと多機能ファイバの複合化により、オールインワンプローブ型のイオン可視化ツールを実現した。
てんかんモデルラットの海馬回路のpH変化をリアルタイムで可視化
開発されたpH可視化プローブは、時間分解能が30ms、空間分解能が250 µmであり、従来の方法では困難だった高時間分解能と高空間分解能の両立を可能とした。このpH可視化プローブについて検証したところ、脳深部の海馬において、疼痛刺激に伴うpHの微小変化を世界で初めてリアルタイムに補捉することに成功した。さらに、海馬回路への光刺激によっててんかんを起こす遺伝子組み換えラット(Thy1-CHR2V)を用い、病態における脳深部海馬回路のpH変化をリアルタイムで可視化することにも成功した。
新規開発したオールインワンプローブ型のイオン可視化ツールは、多機能ファイバと光アドレス型半導体センサを組み合わせることにより、多機能ファイバ本来の機能にイオンイメージング機能を付与し、ファイバや半導体センサ単体だけでは実現できない飛躍的な機能を集積した発明といえるという。「開発したイオン可視化ツールは、斬新な脳機能研究を発展させることができ、これまでに解明されてない病気の原因や治療法の研究において重要な貢献になると考えられる。今後も、てんかんの病理や新たな予防・治療方法につながっていくと期待される」と、研究グループは述べている。
▼関連リンク
・東北大学 プレスリリース








