HIV-1のmRNAに結合する感染抑制タンパク質を探索
京都大学は5月28日、エイズ発症の原因となるヒト免疫不全ウイルス1型(HIV-1)の感染を抑制する新たな宿主タンパク質としてN4BP1を同定し、その分子メカニズムを明らかにしたと発表した。この研究は、同大学院医学研究科の竹内理教授らの研究グループが東京大学、横浜市立大学、大阪大学、独ウルム大学と共同で行ったもの。研究成果は「Nature Microbiology」に掲載されている。
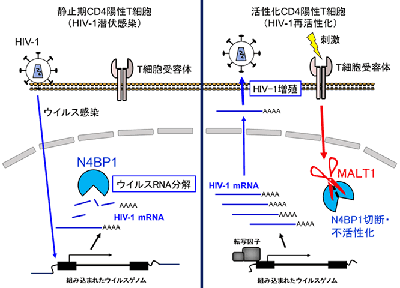
画像はリリースより
HIV-1は、免疫細胞であるCD4陽性T細胞やマクロファージに感染しで増殖する。近年の抗ウイルス療法の発展により、ほとんどのエイズ症例でHIV-1の増殖を抑制することが可能となったが、体内に潜伏感染しているHIV-1を完全に排除することはできず、治療を中断するとすぐにウイルスが再活性化し増殖することがわかっている。現在、HIV-1潜伏感染細胞(リザーバー)を排除し、エイズを根治に導く方法の開発に向けてさまざまな研究が進められている。
ヒト細胞は、APOBEC3やテザリンなど、HIV-1感染を抑制するさまざまな防御因子を有している一方で、これらの宿主防御因子はウイルスタンパク質により抑制されるため、HIV-1と宿主免疫系のせめぎ合いが行われている。これまで明らかとなっている宿主防御因子は、HIV-1感染初期のステップや、ウイルス遊離を抑制するものがほとんど。そこで今回の研究では、ウイルスmRNAに結合し HIV-1 感染を抑制する新たな宿主因子の同定を目的として研究が行われた。
新たなHIV-1感染抑制タンパク質としてN4BP1を同定
研究グループはまず、RNAと結合することが予想される構造をもつ62種類のタンパク質(RNA結合タンパク質:RBP)を、HIV-1を発現するDNAと共に細胞に導入し、HIV-1産生量を比較。多くのRBPの強制発現は、HIV-1産生に影響を与えなかったが、その中でN4BP1というタンパク質を発現させることで、ウイルス増殖が20分の1以下に抑制されることを見出した。さらに調べたところ、N4BP1の発現は、さまざまな種類のHIV-1株を抑制することができ、また、T細胞株やヒトマクロファージにおいてN4BP1を欠損させることにより、HIV-1感染に対し有意に易感染性となることがわかった。N4BP1は、RNA分解酵素として機能する領域を持ち、核内に存在するタンパク質。実際に、HIV-1 RNAに結合し、これを分解する活性を持つこと、RNA分解酵素活性を持たない変異N4BP1がHIV-1を抑制しないことを確認した。また、N4BP1はインフルエンザウイルスなどの感染を抑制することは出来ず、宿主の1型インターフェロン産生にも変化を与えないことから、N4BP1はHIV-1 mRNAを直接認識し分解することで、ウイルス増殖を抑えていると考えられるという。
これまでに明らかとなっている宿主HIV-1防御因子の多くは、HIV-1タンパク質により抑制されるものだったが、N4BP1はHIV-1タンパク質による抑制は認められなかった。一方で、T細胞をT細胞受容体やphorbol 12-myristate 13-acetate(PMA)などの刺激で活性化すると、N4BP1タンパク質が切断を受け、HIV-1抑制能を失うことがわかった。この切断は、T細胞受容体刺激で活性化するタンパク質分解酵素MALT1により行われる。MALT1は、ヒトN4BP1タンパク質を509番目のアルギニン残基の後ろで切断することがわかり、このアルギニンをアラニンに置換した変異体は、MALT1によっても切断されないことが判明した。
新たなエイズ治療の開発に期待
最後に、JNLGFP細胞を始めとしたHIV-1潜伏感染細胞株をPMA刺激して再活性化させたところ、MALT1によるN4BP1分解が起こる事を見出した。さらに、MALT1により分解されない変異N4BP1は、HIV-1潜伏感染細胞のPMA刺激による再活性化を抑制することから、MALT1によるN4BP1分解は、HIV-1潜伏感染細胞の再活性化に寄与することが明らかとなった。
今回の研究では、HIV-1 RNAを標的とした新たな宿主抑制因子としてN4BP1が同定された。また、MALT1によるN4BP1の分解が、HIV-1潜伏感染細胞の再活性化に寄与することが明らかとなった。「N4BP1の役割を検討することで、HIV-1感染やその潜伏感染、再活性化機構のさらなる病態解明に発展することが期待されるとともに、MALT1やN4BP1の機能を調節することで、例えばHIV-1潜伏感染細胞を再活性化させ抗ウイルス治療に対し効果を示すように制御するショック&キル療法など、新たなエイズの治療につながることが期待される」と、研究グループは述べている。
▼関連リンク
・京都大学 研究成果



