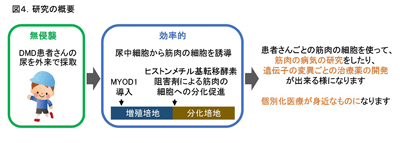
尿中細胞を使ってエクソン・スキップ薬の効果を検証
国立精神・神経医療研究センター(NCNP)は3月6日、難病のデュシェンヌ型筋ジストロフィー(DMD)患者の尿に含まれる細胞を使って、無侵襲で、かつ効率的にエクソン・スキップ治療の効果を検証するダイレクト・リプログラミング方法を確立したと発表した。この研究は、同センター神経研究所遺伝子疾患治療研究部の滝澤歩武研究員、青木吉嗣室長らの研究グループによるもの。研究成果は「Scientific Reports」に、3月7日付で掲載された。
画像はリリースより
DMDは、筋力が低下する遺伝性の難病で、全世界で出生男児4,000~5,000人のうち1人の割合で発症する。現在、これまでステロイド剤以外の治療法がほとんどなかった同疾患を対象に、モルフォリノ核酸(細胞毒性等を克服した第3世代アンチセンス)を用いた「エクソン・スキップ治療」の開発が進んでいる。エクソン・スキップ治療は、アンチセンス核酸を用いて、メッセンジャーRNAのうち、タンパク質に翻訳される領域(エクソン)の一部を人為的に取り除く(スキップする)ことで、アミノ酸読み取り枠のずれを修正(イン・フレーム化)する治療法。正常なジストロフィンタンパク質に比べると、その一部が短縮するものの、機能を保ったジストロフィンタンパク質が発現し、筋機能の改善が期待できる。
DMDに対する新しい治療薬の開発や治療対象を選ぶ際には、患者由来の細胞を用いた薬効評価が必要となる。同研究グループはこれまでに、患者に対して局所麻酔下に皮膚生検を行い、皮膚由来の線維芽細胞を採取して、筋制御因子であるMYOD1を導入して疾患筋細胞(筋管)に分化させ、薬剤の効果を細胞で評価する方法を確立している。しかしながら、この方法は線維芽細胞を得るために侵襲的な皮膚生検を行う必要があった。一方、最近では患者由来の細胞を無侵襲に採取する方法として、尿中に含まれる腎・尿路系上皮細胞(尿中細胞)が注目されている。しかし、MYOD1による筋細胞(筋管)への誘導効率が不十分で、エクソン・スキップ薬等の薬効評価に応用できるかについてはこれまで検証されていなかった。
高効率に筋管分化を誘導し、薬効評価に成功
今回研究グループは、新しくTet発現誘導システムを活用したMYOD1レトロウイルスベクターを作成し、患者由来の尿中細胞を対象に、無侵襲で、かつ効率的なエクソン・スキップ薬等の細胞評価系を確立することを目的に研究を行った。まず、健常人の尿を用いて、安定に尿中細胞を分離・培養できることを確認した。次に、尿中細胞にMYOD1を導入し、分化培地中で疾患筋細胞(筋管)に分化させた。その際、ヒストンメチル基転移酵素阻害剤である3-deazaneplanocin A hydrochloride(DZNep)を分化培地に添加することで、筋管への分化に重要なMYOGENIN遺伝子の発現が有意に促進され、筋管形成までの時間が短縮するばかりか筋管分化度が著しく向上することを見出した。
そこで、エクソン・スキップ薬の効果を、実際にこの筋管で評価可能かを調べるため、さまざまなDMD遺伝子の欠失変異を有する複数の患者から採取した尿中細胞を培養し、筋管に分化させた。これらの筋管を対象にエクソン・スキップを行ったところ、薬物用量に依存してジストロフィンのメッセンジャーRNAがイン・フレーム化し、ジストロフィンタンパク質が回復した。
今回の研究成果で得た方法を用いれば、特定のDMD遺伝子変異をもつ疾患筋細胞(筋管)を対象に、患者ごとの病態研究や、エクソン・スキップを効率的に誘導可能な薬剤スクリーニングなどの治療法開発に応用することが可能だという。さらに、DMD患者に負担をかけることなく、患者由来の疾患筋細胞を効率的に誘導できるため、プレシジョン医療による病態・治療研究が加速する事が期待されると研究グループは述べている。



