副腎に生じる「副腎脂肪腫」、発症メカニズムは不明だった
東京科学大学は9月29日、副腎細胞が脂肪細胞に変わる仕組みを世界で初めて明らかにしたと発表した。この研究は、同大総合研究院難治疾患研究所 病態生理化学分野の柳井翔吾日本学術振興会特別研究員、佐々木純子教授、佐々木雄彦教授らの研究グループによるもの。研究成果は、「PNAS(米国科学アカデミー紀要)」に掲載されている。
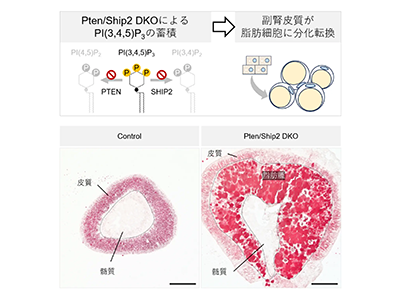
画像はリリースより
(詳細は▼関連リンクからご確認ください)
副腎は、コルチゾールなど生命維持に必須のホルモンを産生し、ストレス応答や代謝調節において全身の恒常性維持に直結する重要な臓器である。通常、副腎には脂肪細胞やその前駆細胞は存在せず、内分泌器官として特化した構造を持っている。しかし、臨床では副腎に脂肪組織が出現する「副腎脂肪腫」と呼ばれる良性腫瘍が報告されてきた。この腫瘍は比較的まれな疾患とされるが、画像診断技術の発展に伴い偶発的に発見される機会が増えており、内分泌疾患の臨床現場においても一定の重要性を持ち始めている。
一方で、副腎に本来存在しない脂肪細胞がなぜ出現するのか、その発症メカニズムは長らく不明だった。実験動物でも同様の病態を再現するモデルは存在せず、分子基盤を明らかにすることは困難だった。そのため、臨床現場では診断がついても治療は外科的切除に依存せざるを得ず、分子機構に基づく新しい治療戦略の開発には至っていなかった。
リン脂質の異常蓄積により副腎皮質細胞が異所性脂肪に変化
今回の研究では、細胞膜のリン脂質PI(3,4,5)P3を分解する酵素PTENとSHIP2を副腎皮質で特異的に同時欠損させたマウスを作製し、副腎におけるPI(3,4,5)P3の異常蓄積を再現した。その結果、副腎皮質細胞は通常のステロイド産生細胞としての特徴を失い、細胞増殖や代謝制御に関わる主要なシグナル伝達経路であるAKT経路が持続的に活性化した。それとともに、転写因子PPARγが異所性に発現し、脂肪細胞様の形質を獲得することが観察された。
さらに、詳細な細胞系譜解析(lineage tracing)を行ったところ、この脂肪細胞様に転換した細胞が副腎皮質の「X-zone細胞」に由来することが判明した。X-zoneはマウスの加齢や性ホルモンの影響で変化する領域として知られていたが、脂肪腫形成に直接関与することが示されたのは今回が初めてである。
AKT経路の抑制により脂肪腫形成の阻止に成功
次に、この現象が実際にAKT経路に依存しているかを検証するため、三重遺伝子改変(トリプルノックアウト)解析を実施した。その結果、AKT経路を抑制すると脂肪腫形成が阻止されたことから、PI(3,4,5)P3の異常蓄積がAKT-PPARγ転写制御を介して、副腎脂肪腫形成を駆動することが証明された。
以上の結果から、副腎脂肪腫の発症メカニズムが分子レベルで初めて明らかになった。このことは、単なる希少疾患の理解にとどまらず、ストレス応答と内分泌機能の破綻がどのように病態形成に結びつくかを考える上で大きな意味を持つ。さらに、従来は外科的切除しか選択肢がなかった副腎脂肪腫に対して、PI3K-AKT-PPARγ経路を標的とした分子治療という新しい戦略につながる可能性がある。
脂質による細胞リプログラミングを実証、再生医療・がん研究にも新たな視点
今回の研究は、これまで実験動物では再現できなかった副腎脂肪腫の形成過程を忠実にモデル化し、脂質シグナルが細胞運命を転換させる分子基盤を明らかにした。この成果は、細胞運命を非遺伝的に制御できる内因性脂質シグナルの存在を初めて実証し、再生医療やがん研究に新たな概念を提示するものである。
同研究で明らかにしたPI(3,4,5)P3/AKTを軸とする脂質シグナルによる細胞運命転換は、副腎脂肪腫の枠を超え、老化や社会的ストレスが内分泌-代謝系に及ぼす影響の理解にも直結すると考えられる。とりわけ、加齢によって視床下部-下垂体-副腎(HPA)軸の反応性やコルチゾールの日内リズムが乱れ、慢性的な社会的ストレスによる負荷が増大し、代謝・免疫・神経系の脆弱性が高まることが報告されている。今後は、副腎が担うストレス応答と脂質シグナルのクロストークを、加齢に伴う内分泌環境の変化や生体ロバストネスの低下と結びつけて検証し、慢性的な社会的ストレスがPI(3,4,5)P3/AKT経路や転写制御機構に与える影響を、多層オミクス解析により明らかにしていく必要がある。
PI3K-AKT-PPARγ経路を標的とした治療戦略、バイオマーカーに期待
「副腎以外の臓器における病的脂肪化や脂肪腫でも同様のメカニズムが作動するかを横断的に評価し、脂質シグナルを介した細胞リプログラミングを一般原理として定式化することを目指す。これにより、PI3K-AKT-PPARγ経路を標的とした治療戦略の開発や、バイオマーカーによる層別化・予防介入の実現が期待される」と、研究グループは述べている。
▼関連リンク
・東京科学大学 プレスリリース



