アラブ首長国連邦アブダビ

(ビジネスワイヤ) — COVID-19と闘うためのシノファーム(中国医薬集団)CNBG(中国生物技術集団)の不活化ワクチンを対象とし、世界保健機関(WHO)の協力を得た初の世界的第3相臨床試験が、アブダビにて、国際連携活動を通じてこの世界的流行病を克服するというUAE指導者層の約束に基づき、開始されました。
本プレスリリースではマルチメディアを使用しています。リリースの全文はこちらをご覧ください。:https://www.businesswire.com/news/home/20200719005070/ja/
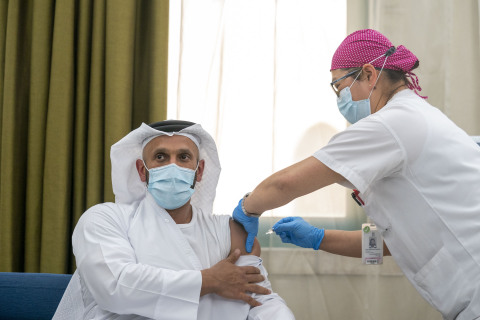
H.E. Sheikh Abdullah bin Mohammed Al Hamed, Chairman of Department of Health, Abu Dhabi, being administered the world’s first clinical Phase III trial of inactivated vaccine to combat COVID-19 (Photo – AETOSWire).
アブダビ保健局長のシェイク・アブドゥラ・ビン・ムハンマド・アル・ハメド閣下は、COVID-19に対する不活化ワクチンの第3相試験を世界で初めて開始しましたが、本試験の開始はアブダビを拠点とするG42ヘルスケアと、世界で6番目に大きいワクチンメーカーであるシノファームCNBGとの間の協業成果です。
UAEが本試験を実施する国に選ばれたのは、200を超える国籍の人々がUAEに居住しており、さまざまな民族を対象に充実した研究が可能で、世界各国へ適用できる実現可能性が高いからです。試験を実施するのは、臨床施設を提供しているアブダビ医療サービス会社(SEHA)です。
UAEの各保健当局は、最大1万5000人のボランティアが参加する許可を与えており、G42ヘルスケアとSEHAは、WHOと米国食品医薬品局(USFDA)が規定した国際的ガイドラインに従ってアブダビ保健局とSEHAが監督する試験に最低5000人を参加させるべく、活動しています。
UAE国家COVID-19臨床管理委員会委員長であるDr.ナワル・アーメド・アルカービは、次のように述べています。「本試験に参加することで、COVID-19の世界的流行病との世界的な闘いに大きく貢献することができます。私たちは、成功すればワクチンの製造につながる試験プロセスを促進できることを光栄に思います。」
本試験は、シノファームが中国で実施した第1相試験および第2相試験の成功に続くものであり、これらの試験ではボランティアの100%が抗体を作り出しました。
G42ヘルスケアのアシシュ・コーシー最高経営責任者(CEO)は、次のように述べています。「当社はこの画期的な第3相臨床試験でシノファームCNBGと提携でき大変光栄です。G42ヘルスケアは当社のAIソリューション、スーパーコンピューター、先進的なCOVID-19診断ソリューションを使用して、これら試験の臨床業務の実施を担います。」
シノファームCNBGのバイオ医薬品担当プレジデントを務めるJingjin Zhuは、次のように付け加えています。「UAEはイノベーションと寛容の国であり、世界中からのあらゆる民族的背景の人々が住んでいます。当社はパートナーのG42ヘルスケアと緊密に協力し、アブダビの保健当局の支援を受けて、これら臨床試験を成功裏に完了し、世界中で必要としている人々がこのワクチンを利用できるようにしたいと思います。」
*出典:AETOSWire
本記者発表文の公式バージョンはオリジナル言語版です。翻訳言語版は、読者の便宜を図る目的で提供されたものであり、法的効力を持ちません。翻訳言語版を資料としてご利用になる際には、法的効力を有する唯一のバージョンであるオリジナル言語版と照らし合わせて頂くようお願い致します。
businesswire.comでソースバージョンを見る:https://www.businesswire.com/news/home/20200719005070/ja/
CONTACT
Tasneem Riyaz
g42@apcoworldwide.com





