特発性肺線維症での肺腔内におけるACE2発現を解析
名古屋市立大学は11月11日、特発性肺線維症のマウスモデルおよび患者サンプルを用いて肺腔内におけるACE2発現に関する研究を行い、同疾患の患者が、新型コロナウイルス(SARS-CoV-2)感染により高感受性であることを示した一方、急性肺炎時は肺腔内におけるウイルス感染可能な領域はむしろ狭まる傾向にあることがわかったと発表した。この研究は、同大大学院医学研究科神経発達症遺伝学の三浦陽子研究員、金澤智助教らの研究グループと、オーストラリアのモナーシュ大学によるもの。研究成果は、「Frontiers in Immunology」に掲載されている。
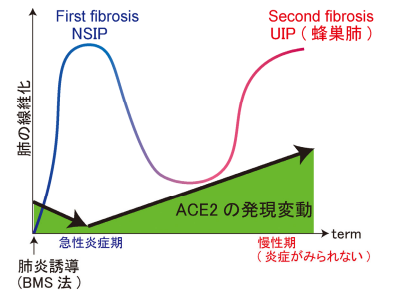
画像はリリースより
(詳細は▼関連リンクからご確認ください)
特発性肺線維症の患者は、SARS-CoV-2感染に対し、より高い感受性を有するのではないかと危惧されていた。またSARS-CoV-2感染により引き起こされる急性肺炎によるサイトカインストームが、肺腔内で発現しているACE2(SARS-CoV-2感染の細胞内への入り口となるアンジオテンシン変換酵素2)の発現量を上昇させ、感染領域を広げる可能性が示唆されていた。そこで研究グループは、独自に開発した特発性肺線維症マウスモデル(induced-usual interstitial pneumonia;iUIP、特発性間質性肺炎)および患者サンプルを用いて、肺腔内におけるACE2発現に関する研究を進めた。また感染により引き起こされる病態生理学的状態を、PCLS(Precision-cut lung slices、肺臓の薄切組織)を用いたex vivo培養システムの中で再現し、肺におけるACE2発現の変化を検証した。
慢性期の患者でACE2高発現、急性炎症期ではACE2発現量減少
iUIPマウスモデルおよびヒト患者検体を調べた結果、慢性的な肺線維症状態にある特発性肺線維症では、ACE2の発現量が非病態時より多いことから、SARS-CoV-2感染のリスクが高いことがわかった。一方、急性炎症期に、ACE2の発現量はむしろ減少することがわかった。このことから急性炎症期において、肺腔内における感染領域はむしろ減少していることが示唆された。
ACE2は異常性を獲得した上皮細胞に発現
先行研究で、iUIPマウスモデルにおいて肺炎慢性期、浸潤性を獲得した異常な上皮細胞が観察されることがわかっていた。今回の研究では、この異常上皮細胞の約20%でACE2発現が観察された。そして、これらの上皮細胞では、上皮細胞自身の極性が消失している可能性が示唆された。具体的には、細気管支領域ではACE2発現は気道面に発現している一方、浸潤性を獲得した異常上皮細胞ではACE2発現に一定の方向性が見られなかった。特発性肺線維症の患者肺においても肥厚した上皮細胞に加え、浸潤性の上皮細胞も確認される。これらの上皮細胞でもマウスモデル同様、異所性のACE2発現が観察された。
急性炎症時、IL-6やインターフェロン、ウイルス感染そのものによりACE2発現減少
急性炎症時、肺におけるACE2発現量が下がる理由を探るため、SARS-CoV-2感染時の病態生理学的状態(各種サイトカイン、低酸素状態)が肺に及ぼす影響をPCLS、ex vivo培養システムを用いて検討した。その結果、インターロイキン6(関節リウマチ治療薬を転用できるかもしれないとの観測で、COVID-19治療に関するニュースなどで話題になった)、ウイルス感染により誘導産生されるインターフェロン、ウイルス感染そのもの(実験ではウイルス感染状態を疑似的に再現している)により、ACE2の発現量はむしろ減少することが明らかになった。
ニンテダニブ投与によりACE2発現量減少
また、間質性肺炎下で肺は低酸素状態になると考えられているが、このような低酸素環境もACE2発現量を減少させることがわった。間質性肺炎治療に用いられる代表的な治療薬、ピルフェニドン、ニンテダニブが、ACE2発現に影響を及ぼすのか否かについても検討したところ、ピルフェニドン投与による影響は見られなかった一方、ニンテダニブ投与により ACE2発現量が減少することがわかった。
PCLSを用いたex vivo培養、さまざまな研究開発へ応用可
今回の研究では、特発性肺線維症マウスモデル由来のPCLSを用いたex vivo培養を樹立した。PCLSに関する一連の研究は、オーストラリア・メルボルンのモナーシュ大学との共同研究が進んでいる。このシステムを利用することで、使用する動物の数を減らし、より効率的に作用物による肺への影響を評価することができることを示した。研究グループは今後、この技術を応用し、肺に対する毒性試験、抗がん剤による線維化の評価、肺線維症に対する治療薬開発など多岐に渡る応用研究を進めていく予定だとしている。
特発性肺線維症は新型コロナに対して警戒すべき疾患であることを示唆
研究グループが開発したiUIPマウスモデルは、肺に強い炎症を惹起した後にIPF様の症状を呈する。このマウスモデルと患者検体を用い、特発性肺線維症ではSARS-CoV-2感染リスクが高い可能性を示した。今回のデータが、「SARS-CoV-2感染に対し、特発性肺線維症患者の重症化リスクは高い」という結論に直接結びつくものではないが、肺腔内におけるSARS-CoV-2感染可能領域がより広がっていることから、警戒すべき疾患であると考える必要がある。
「SARS-CoV-2感染治療薬の開発は、ワクチン開発に対し、大きく立ち遅れている。今回の研究成果には、新たな治療薬開発のヒントとなるデータが多く含まれている。特に、PCLS、ex vivo培養システムは、感染症の治療薬開発だけでなく、間質性肺炎治療薬開発、肺に対する毒性試験など重要な検討項目を評価するための、強力なツールになる可能性がある」と、研究グループは述べている。
▼関連リンク
・名古屋市立大学 プレスリリース








