AIを用いて読影と画像解析を自動化、認知症の全自動診断に向けた基幹技術開発を目指す
量子科学技術研究開発機構(量研)は8月29日、脳内に蓄積する異常タンパク質「タウ」病変のPET画像を人工知能(AI)で解析することにより、アルツハイマー病や前頭側頭葉変性症など、多様な神経変性型の認知症に生じる特徴的な脳内の病態を自動的に認識し、認知症の診断と鑑別に役立つスコアを算出することに成功したと発表した。この研究は、量研量子生命・医学部門 量子医科学研究所 脳機能イメージング研究部の樋口真人部長、遠藤浩信研究員らの研究グループによるもの。研究成果は、「Movement Disorders」オンライン版に掲載されている。
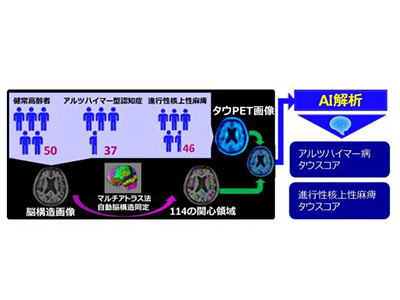
画像はリリースより
(詳細は▼関連リンクからご確認ください)
日本では2012年に約460万人が、高齢化が進む2040年には800万人以上が認知症を発症すると推計されている。しかし、根本的な治療法は開発されておらず、進行を止めることができないため、本人のみならず介護者、家族、社会全体に身体的、心理的、社会的、経済的影響を及ぼす。
認知症の大半を占めるのは、脳の中に異常なタンパク質が蓄積する神経変性型の認知症で、これはアルツハイマー病、前頭側頭葉変性症、レビー小体型認知症の3大認知症から成る。さらに、アルツハイマー病と前頭側頭葉変性症ではアミロイドβ(Aβ)やタウを主とする異常タンパク質が脳内に蓄積し、これらの異常タンパク質の蓄積に伴い神経細胞が死ぬことで、物忘れ、運動障害、精神症状などの多彩な症状が出現する。この異常タンパク質の蓄積を抑えることが、根本的な治療に不可欠と考えられる。
認知症の症状は症例ごとに多様である一方、異なる疾患でも同様の症状を呈することがあり、症状のみで早期診断することはできない。そのため、早期診断には異常タンパク質の蓄積を可視化するイメージング技術が極めて効果的と言える。こうした状況をふまえ、研究グループは、アルツハイマー病や進行性核上性麻痺などの異常なタウ蓄積を高いコントラストで捉えることのできるPET薬剤「[18F]PM-PBB3 (一般名:florzolotau)」を開発した。しかし、PET画像から診断に役立つ情報を得るためには、熟練を要する読影技術や画像解析技術が必要だった。だが、AIを用いることで読影と画像解析を自動化できれば、診断に役立つだけでなく、さまざまな研究機関や製薬企業によって開発が進められているタウ病変を減らす新たな認知症治療薬の薬効評価を自動化することも可能になると見込まれる。しかし、自動化には「各認知症のタウPET画像上において、どの脳領域が診断に最も役立ち、疾患の重症度や治療効果の評価に有用なのか不明」「正確にタウPET画像を自動で評価する方法がない」という2つの課題があった。
研究グループはこれらの課題を解決すべく、AIを用いて読影と画像解析を自動化し、PET画像のアルツハイマー病らしさを表す「アルツハイマー病タウスコア」と、進行性核上性麻痺らしさを表す「進行性核上性麻痺タウスコア」をそれぞれ算出できるように、認知症の全自動診断に向けた基幹技術の開発を目指した。
AIで「アルツハイマー病タウスコア」と「進行性核上性麻痺タウスコア」を算出
タウPET画像を診断や治療効果の評価に用いるためには、疾患に特徴的なタウ蓄積パターン特定と、正確な定量が不可欠だ。画像からPET薬剤の集積を定量化する際、現在の最も信頼できる基準は、関心領域を手動で定義して測定することだが、臨床試験における大規模なデータセットを解析するためには多大な労力を必要とする。また、定性的な評価では評価の恣意性や再現性に問題が残るため、コンピュータプログラムを用いた自動定量法が用いられるようになり、自動で全脳の関心領域を同定する方法も開発されている。
ヒトの脳は大きさや形状に個人差があるため、関心領域を自動で同定するには、被検者の脳画像を標準脳に合わせて解析する必要がある。ところが、各被検者データを1つの標準脳マップへ合わせて解析を行う場合(シングルアトラス法)には、個人差に加えて病気による脳萎縮もあり、将来的な臨床試験で求められる精度を維持して脳病態の客観的評価指標を確立することは困難だった。そこで今回、関心領域を自動で同定する方法として、あらかじめ脳画像の構造を正確に同定した複数人のマルチアトラスを教師データとして用い、AIにより各被験者の脳画像の構造を自動で同定するマルチアトラス法をPET画像に適用し、臨床試験で求められる精度と解析の簡便性を担保した。さらに、タウ蓄積パターンの評価においては、臨床診断に関連する重要な情報を抽出し、検証ステップを含むAIが必要となるため、エラスティックネット線形分類解析というAIの手法を用いた。同手法は多数の脳領域のタウPETの値から疾患を特定するために有効な領域を選択し、重要度の重み付けを行うだけでなく、診断に貢献度の低い領域については削減し、疾患ごとのタウ蓄積パターンを探し出すことができる。また、少数のタウPETデータセットであっても堅牢なパターン認識モデルを作成することができ、高い解釈性・説明性を実現することが可能となる。
同研究では、アルツハイマー型認知症患者(Aβ陽性の軽度認知機能障害患者含む)37人、進行性核上性麻痺患者46人、健常高齢者50人を対象に、[18F]PM-PBB3を投与して撮影した画像にマルチアトラス法を適用し、脳内114か所の関心領域におけるPET薬剤集積値を解析した。そして、AIを用いてアルツハイマー型認知症と進行性核上性麻痺を区別するために最適化された線形関数を求め、解析で得られたPET薬剤集積値を線形結合することで、各被検者の「アルツハイマー病らしさ」を表す「アルツハイマー病タウスコア」と「進行性核上性麻痺らしさ」を表す「進行性核上性麻痺タウスコア」を算出した。
アルツハイマー病タイプの正解率は約98%、進行性核上性麻痺タイプの正解率は約95%
健常高齢者、アルツハイマー型認知症患者、進行性核上性麻痺患者において、高精度に同定した114の脳構造領域についてタウPET集積値を定量し、それらの値を有効な学習用データとして用いることで、疾患に特徴的な領域のタウPET集積値を個人ごとにタウスコアとして算出。学習用データ対検証用のテストデータにランダムに10回分に分け、繰り返し検討して最適な線形モデル関数を作成しテスト用データで評価した結果、アルツハイマー病タイプのタウスコアの疾患分類における正解率は98.6±0.02%(平均±標準偏差)、進行性核上性麻痺タイプのタウスコアの正解率は95.0±0.02%(平均±標準偏差)だった。
タウスコアの高いアルツハイマー型認知症患者と進行性核上性麻痺患者のそれぞれのタウ蓄積パターンを平均化してみると、前頭葉など一部に重なりがみられるところがあるが、タウスコアを決定するためのAIモデルにおいて、アルツハイマー病タイプでは扁桃体など、内側側頭葉をはじめとする大脳領域で、進行性核上性麻痺タイプでは淡蒼球や中脳など深部脳領域でタウ蓄積が認められた。このことから、アルツハイマー病タウスコアでは、内側側頭葉などの大脳領域が、進行性核上性麻痺タウスコアでは深部脳領域が、それぞれ疾患分類に重要であることが確認された。
タウスコアの高さは、疾患の重症度の尺度としても有用な可能性
次に、それぞれのタウスコアと臨床症状との関連を見たところ、アルツハイマー病患者と認知テストで失点があった健常高齢者のアルツハイマー病タウスコアが高いほど認知機能の障害が重度であり、進行性核上性麻痺患者の同タウスコアが高いほど運動障害が重度だった。本来病気を区別するためにAIで計算したタウスコアが病気の重症度と有意な相関を示したことから、タウ病変の重要性が病気の診断にも症状にも関連している可能性が示された。
さらに、今回PET検査を行った症例とは異なる、すでに亡くなっている患者脳切片に対してPM-PBB3の結合を検討してみたところ、PET検査の結果と同様、淡蒼球や扁桃体には多量の脳内タウ蓄積を認め、PM-PBB3が結合していることが確認された。
[18F]PM-PBB3の診断薬としての承認を得るためのP1/P2臨床試験が進行中
今回の研究で、それぞれアルツハイマー病らしさと進行性核上性麻痺らしさのタウ蓄積の脳内分布を生体内で高性能に区別できるタウスコアをAIモデルが作成された。これにより、熟練を要する読影や画像解析のスキルが再現され、認知症の全自動診断に向けた基幹技術がもたらされた。同技術は症例数を増やすことでモデルの改良が可能であり、他のタウ病理を特徴とする認知症の画像を組み込んで学習させることで、その病気らしさを区別するタウスコアを計算できると期待される。なお現在、APRINOIA社との共同で、米国、台湾、日本などで[18F]PM-PBB3の診断薬としての承認を得るための第1相および第2相臨床試験が進行中だ。
「タウ病変に対する抗体を含む治療薬候補が世界各地で開発されているため、今後、ますます[18F]PM-PBB3の需要は高まるものと考えられ、さらに本研究によるAI解析技術を応用することにより、タウスコアによる診断が確実な方の治験へのリクルートのみならず、こうした治療薬の薬効評価を自動化することも可能になると見込まれる」と、研究グループは述べている。
▼関連リンク
・量子科学技術研究開発機構 プレスリリース








