成熟膵島細胞は自己複製能がほぼなく、iPS由来インスリン産生細胞は機能的に未熟
東京大学医科学研究所は2月11日、出生前後に増殖する膵島細胞で高発現するMYCLに着目し、MYCLを働かせることで生体内外の成熟膵島細胞に活発な自己増殖を誘発できることを明らかにしたと発表した。この研究は、同研究所先進病態モデル研究分野の平野利忠大学院生、山田泰広教授、京都大学、愛知医科大学ほかの研究グループによるもの。研究成果は、「Nature Metabolism」オンライン版に掲載されている。
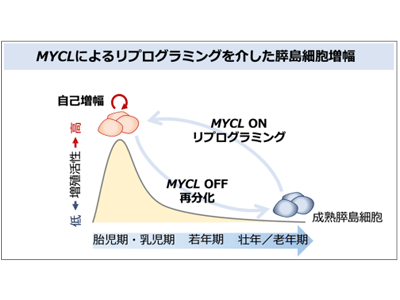
画像はリリースより
(詳細は▼関連リンクからご確認ください)
世界の糖尿病患者数は生活習慣や社会環境の変化により急速に増え続けており、現在の糖尿病人口は4億人を超えると推定される。糖尿病は網膜症、神経障害に加えて腎障害等の合併症を引き起こし、人工透析が必要となることもある。また、世界における糖尿病およびその合併症に対する医療費は年間90兆円とされており、糖尿病による医療費圧迫が大きな社会問題となっている。
糖尿病は膵臓に存在する膵島β細胞から分泌されるインスリンの絶対的もしくは相対的不足により発症する。成人膵島細胞には自己複製能がほとんどないことから、膵島細胞の機能は再生しない。現在の糖尿病に対する治療法は、糖の吸収を抑える薬剤やインスリン製剤の投与等の対症療法が主流であり、そのほとんどが糖尿病そのものを治療するものではない。糖尿病の根治を目指してiPS細胞などの多能性幹細胞からインスリン産生細胞を作製し、細胞移植による再生医療に応用する取り組みも進められているが、多能性幹細胞由来のインスリン産生細胞は、機能的に未熟であることが大きな問題となっており、医療応用に至っていない。今回、研究グループは、出生前後の膵島細胞が自己複製能を持つことに着目し、成熟した膵島細胞の自己増幅技術の開発を目指した。
成熟膵島細胞にMYCL発現<遺伝子発現状態が胎生期様にリプログラミング<増殖
膵島細胞は出生前後において活発に増殖する一方で、発生とともにその増殖能は急激に失われ、成熟した膵島細胞には自己複製能がほとんどないことがわかっている。そこで研究グループは、増殖する膵島細胞の特性を理解し、成熟膵島細胞の増殖誘導に応用するために、胎生期のマウス膵臓における1細胞遺伝子発現解析を行った。増殖誘導活性を持つMYCファミリー遺伝子群(MYC、MYCN、MYCL)に着目したところ、膵島細胞に限局してMYCLが発現していると判明。また、ヒトiPS細胞から膵島細胞様細胞への分化過程においても、膵島前駆細胞でMYCLが一過性に発現していることがわかった。さらにMYCL遺伝子を破壊したマウスでは出生前後の膵島細胞で増殖活性が低下することを発見した。このことから、MYCLが発生・分化過程における膵島細胞の増殖を制御することが明らかとなった。
研究グループは次に、MYCLを膵島細胞へ発現させることで、成熟膵島の自己増殖の誘導を試みた。まず、成体マウスより単離した膵島細胞に、試験管内でMYCLの発現誘導を行ったところ、活発な細胞増殖が誘導された。また、加齢したマウスの膵島細胞や、ヒト脳死ドナー由来膵島細胞、さらには、マウスの生体内の膵島細胞においても同様の自己複製の誘導が確認された。MYCLを発現誘導させたマウスおよびヒト膵島細胞の1細胞遺伝子発現解析を行ったところ、MYCLの発現により遺伝子発現状態が胎生期に類似した状態に変化していることがわかった。
これらの結果から、MYCLが成熟膵島細胞の遺伝子発現状態を胎生期様の状態へと「リプログラミング」させ、増殖活性を付与していることが示唆された。
糖尿病モデルマウスの血糖値改善に成功
最後に研究グループは、MYCLにより増幅させた膵島細胞の機能性を評価した。まず、マウスにストレプトゾトシン(STZ、膵島β細胞を特異的に破壊する薬剤)を投与することで糖尿病にさせ、その後生体内においてMYCLの発現誘導を行った。
その結果、MYCL発現誘導後に速やかに血糖値の改善が認められた。また、MYCLにより単離した膵島細胞を試験管内で増幅させたのちに、糖尿病マウスに移植したところ、血糖値の改善が認められた。これらの結果から、MYCLの発現により生体内外で増幅させた膵島細胞が高い機能性を持ち、糖尿病マウスを治療できることが示された。
膵島細胞の再生医療開発への応用に期待
糖尿病を根治させるためには、生体内の膵島β細胞量を増やす必要がある。現在の細胞移植治療は、脳死ドナー由来の膵島細胞を使用するが、ドナー不足が問題となっている。この問題点を改善するために、多能性幹細胞からの分化誘導による膵島細胞の作製による細胞移植治療の開発が盛んに行われている。しかしながら、成熟した機能性の高い膵島細胞の作製はハードルが高く、未だ医療応用に至っていない。
今回の研究では、マウス膵島細胞の発生過程にMYCL遺伝子が発現上昇することが見出され、出生前後の膵島細胞の増殖にMYCL遺伝子が重要な役割を果たすことが示された。さらに、成体マウス生体内において一時的なMYCL遺伝子の発現誘導を行うことで、現在まで不可能であると考えられてきた成熟膵島細胞の増幅に成功した。また生体内で増殖させた膵島細胞は高い機能性を持ち、糖尿病モデルマウスの治療が可能であることが確認された。試験管内においても成熟膵島細胞の自己増殖誘導は可能であり、試験管内で増幅させた膵島細胞の移植によりマウス糖尿病を治療可能であることが示された。さらに、ヒト膵島細胞の分化過程でもMYCL遺伝子が発現上昇すること、MYCL遺伝子の誘導により、脳死ドナー由来のヒト膵島細胞に自己増殖活性を付与できることが示された。
研究グループは今回の研究成果について、「MYCL遺伝子により体外で増幅させた膵島細胞を再び体の中に戻す細胞移植療法や、MYCL遺伝子治療による体内での膵島細胞増幅技術の開発といった、膵島細胞の再生医療開発への応用が期待される」と、述べている。
▼関連リンク
・東京大学医科学研究所 プレスリリース








